노르페티딘
Norpethidine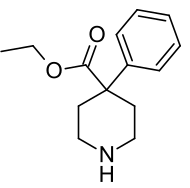 | |
 | |
| 임상자료 | |
|---|---|
| 경로: 행정 | 해당 없음 |
| ATC 코드 |
|
| 법적현황 | |
| 법적현황 | |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| 켐스파이더 | |
| 유니 | |
| 켐벨 | |
| CompTox 대시보드 (EPA) | |
| ECHA InfoCard | 100.000.918 |
| 화학 및 물리적 데이터 | |
| 공식 | C14H19NO2 |
| 어금질량 | 233.311 g·2011−1 |
| 3D 모델(JSmol) | |
| |
| |
| (iii) | |
노르페티딘(Normperidine, pethidine 중간 B)은 4-페닐피페리딘 파생물로, 페티딘(meperidine)의 독성 대사물이다. 그것은 유엔 마약 단일 협약에 의해 예정되어 있다. 그것은 미국의 스케줄 II 마약류 통제 물질이며, ACSCN은 9233이다. 2014년 연간 제조 쿼터는 11g(0.39온스)이었다.[1]
노르페티딘은 페티딘 자체와 다양한 N-대체 파생상품을 제조하는 데 잠재적으로 사용되기 때문에 통제된 약이지만, 그 자체로는 오피오이드 활성도가 거의 없다. 대신 노르페티딘은 흥분제 역할을 하며 경련을 일으킨다.[2][3]
보다 배설되고 있듯이 페티딘 고등 doses[4]에 또는 정맥 infusion,[5]norpethidine에 의해 집행되어 사용되는 몸 안에서 빠른 속도로, 제대로 발휘되지 못하는 간이나 안고 노인들 patients[6]이나 특히에 축적될 수 있을 때 페티딘 약에서 흥미 진통제로 사용된다 norpethidine의 Bioaccumulation은 주요 합병증이다. 신장 씨주로 경련과 근막염[8], 저포나트레미아 등의 다양한 독성 효과를 유발하는 nection.[7][9] 이러한 합병증은 심각할 수 있고 때때로 죽음을 초래하기도 한다.[10]
pethidine to norpethidine의 신진대사는 주로 간에서 CYP2B6, CYP2C19, CYP3A4라는 CYP 효소에 의해 수행되며, 이러한 효소의 활성도는 개인마다 다를 수 있고 다른 약물의 동시 사용에 의해 영향을 받을 수 있기 때문에 노르페티딘의 생성 속도와 정도를 예측하기 어려울 수 있다.[11][12]
노르페티딘은 에톡세리딘,[13] 벤제티딘,[14] 푸레티딘,[15] 모르페리딘, 아닐리딘, 페노페리딘, 피미노딘, 옥페네리딘을 포함한 다른 약물의 합성에 선행으로 사용될 수 있다.
참고 항목
참조
- ^ "Conversion Factors for Controlled Substances". Diversion Control Division. Drug Enforcement Administration (DEA), U.S. Department of Justice.
- ^ Umans JG, Inturrisi CE (October 1982). "Antinociceptive activity and toxicity of meperidine and normeperidine in mice". The Journal of Pharmacology and Experimental Therapeutics. 223 (1): 203–6. PMID 7120119.
- ^ Plummer JL, Gourlay GK, Cmielewski PL, Odontiadis J, Harvey I (January 1995). "Behavioural effects of norpethidine, a metabolite of pethidine, in rats". Toxicology. 95 (1–3): 37–44. doi:10.1016/0300-483x(94)02871-q. PMID 7825188.
- ^ Simopoulos TT, Smith HS, Peeters-Asdourian C, Stevens DS (January 2002). "Use of meperidine in patient-controlled analgesia and the development of a normeperidine toxic reaction". Archives of Surgery. Chicago, Ill. 137 (1): 84–8. doi:10.1001/archsurg.137.1.84. PMID 11772223.
- ^ Stone PA, Macintyre PE, Jarvis DA (November 1993). "Norpethidine toxicity and patient controlled analgesia". British Journal of Anaesthesia. 71 (5): 738–40. doi:10.1093/bja/71.5.738. PMID 8251291.
- ^ Holmberg L, Odar-Cederlof I, Boreus LO, Heyner L, Ehrnebo M. 노인과 젊은 환자의 페티딘과 노르페티딘의 비교 처리. 유럽 임상 약리학 저널 1982;22(2):175-9.
- ^ Pond SM, Tong T, Benowitz NL, Jacob P, Rigod J (August 1981). "Presystemic metabolism of meperidine to normeperidine in normal and cirrhotic subjects". Clinical Pharmacology and Therapeutics. 30 (2): 183–8. doi:10.1038/clpt.1981.146. PMID 7249503. S2CID 10117158.
- ^ Reutens DC, Stewart-Wynne EG (December 1989). "Norpethidine induced myoclonus in a patient with renal failure". Journal of Neurology, Neurosurgery, and Psychiatry. 52 (12): 1450–1. doi:10.1136/jnnp.52.12.1450. PMC 1031622. PMID 2614458.
- ^ Appel WC (November 1987). "Possible roles of normeperidine and hyponatremia in a postoperative death". Canadian Medical Association Journal. 137 (10): 912–3. PMC 1267380. PMID 3676934.
- ^ Jiraki K (March 1992). "Lethal effects of normeperidine". The American Journal of Forensic Medicine and Pathology. 13 (1): 42–3. doi:10.1097/00000433-199203000-00009. PMID 1585886. S2CID 32005631.
- ^ Ramírez J, Innocenti F, Schuetz EG, Flockhart DA, Relling MV, Santucci R, Ratain MJ (September 2004). "CYP2B6, CYP3A4, and CYP2C19 are responsible for the in vitro N-demethylation of meperidine in human liver microsomes". Drug Metabolism and Disposition: The Biological Fate of Chemicals. 32 (9): 930–6. PMID 15319333.
- ^ McHugh GJ (June 1999). "Norpethidine accumulation and generalized seizure during pethidine patient-controlled analgesia". Anaesthesia and Intensive Care. 27 (3): 289–91. PMID 10389564.
- ^ 미국, 2858316, "New piperidine 파생상품" Henri M, 1958년 10월 28일 발행, UCB SA에 할당
- ^ Frearson PM, Stern ES (1958). "622. Some new analogues of pethidine. Part III. 1-Aryloxy-alkylnorpethidines, and close analogues". Journal of the Chemical Society (Resumed): 3065–7. doi:10.1039/JR9580003065.
- ^ Frearson PM, Hardy DG, Stern ES (1960). "426. Some new analogues of pethidine. Part IV. Substituents at the 1-position incorporating cyclic ether groups". Journal of the Chemical Society (Resumed): 2103–7. doi:10.1039/JR9600002103.


