애더럴
Adderall | |
 | |
| 의 조합 | |
|---|---|
| 아스파르트산 1수화물로서의 암페타민 | 25% – 자극제 (12.5% levo; 12.5% dextro) |
| 황산암페타민 | 25% – 자극제 (12.5% levo; 12.5% dextro) |
| 덱스트로암페타민 당산염 | 25% – 자극제 (0% levo; 25% dextro) |
| 황산 덱스트로암페타민 | 25% – 자극제 (0% levo; 25% dextro) |
| 임상자료 | |
| 상호 | 애더럴, 애더럴 XR, 마이데이는 |
| 기타이름 | 혼합 암페타민 염; MAS |
| AHFS/Drugs.com | 모노그래프 |
| 메드라인 플러스 | a601234 |
| 라이센스 데이터 | |
| 의존성 법적 책임 | 보통[3][4] - 높음[5][6][7] |
| 경로 행정부. | 입으로 보면, 절연, 직장, 설하 |
| 드럭 클래스 | CNS 흥분제 |
| ATC코드 | |
| 법적지위 | |
| 법적지위 | |
| 식별자 | |
| CAS 번호 | |
| 펍켐 CID | |
| IUPHAR/BPS | |
| 드럭뱅크 | |
| 켐스파이더 | |
| 유니아이 | |
| 케그 | |
| ChEBI | |
| 쳄블 | |
| (주로) | |
Adderall과 Mydayis는[8] 4개의 암페타민 염을 포함하는 혼합 암페타민 염이라고 불리는 복합 약물의 상호입니다[note 2].이 혼합물은 암페타민과 덱스트로암페타민으로 동등한 비율로 구성되어 있는데, 이 혼합물은 암페타민의 두 거울상이성질체인 덱스트로암페타민과 레보암페타민의 (3:1) 비율을 만듭니다.두 거울상이성질체 모두 자극제이지만,[1][10][11] 각각 이브케오와 덱세드린/젠제디로 시판되는 라세믹 [1][2]암페타민 또는 덱스트로암페타민과는 구별되는 효과 프로필을 애더럴에게 줄 수 있을 정도로 차이가 있습니다.애더럴은 주의력결핍 과잉행동장애(ADHD)와 기면증 치료에 사용됩니다.그것은 또한 운동 능력 향상, 인지 능력 향상, 식욕 억제제, 그리고 즐거움을 주는 것으로서 부정하게 사용됩니다.페네틸아민 [1]계열의 중추신경계 자극제입니다.
애더럴은 일반적으로 ADHD와 기면증의 증상을 치료하는데 잘 견디고 효과적입니다.치료 용량에서 애더럴은 행복감, 성욕의 변화, 각성도 증가, 인지조절 향상과 같은 정서적, 인지적 효과를 유발합니다.이러한 용량에서는 반응시간 단축, 피로저항성, 근력 증가 등의 물리적 효과를 유도합니다.대조적으로, 훨씬 더 많은 용량의 애더럴은 인지 조절을 손상시키고, 급격한 근육 파괴를 일으키거나, 공황 발작을 일으키거나, 정신병(예: 편집증, 망상, 환각)을 유발할 수 있습니다.애더럴의 부작용은 개인마다 매우 다르지만, 가장 일반적으로 불면증, 구강건조증, 식욕부진, 체중감소 등이 있습니다.ADHD 치료를 위해 사용되는 것과 같이 매일 상당히 낮은 용량으로 처방된 대로 애더럴을 사용하는 경우 중독이나 의존증에 걸릴 위험은 미미합니다.더 큰 일일 용량에서 Adderall을 일상적으로 사용하는 것은 고용량에서 나타나는 뚜렷한 강화 효과로 인해 중독 또는 의존의 상당한 위험을 초래합니다.암페타민의 레크리에이션 용량은 일반적으로 처방된 치료 용량보다 훨씬 크며 심각한 [sources 1]부작용의 위험이 훨씬 큽니다.
Adderall(레보암페타민 및 덱스트로암페타민)을 구성하는 두 가지 암페타민계 항이성질체는 뇌의 신경전달물질인 노르에피네프린과 도파민의 활성을 증가시킴으로써 ADHD 및 기면증 증상을 완화시키고,이는 뉴런에서 인간 미량 아민-연관 수용체 1 (hTAAR1) 및 소포체 모노아민 수송체 2 (VMAT2)와의 상호작용으로부터 부분적으로 기인합니다.덱스트로암페타민은 레보암페타민보다 더 강력한 자극제이지만, 레보암페타민은 약간 심혈관 및 말초 효과가 강하고, 제거 반감기가 덱스트로암페타민보다 더 깁니다.Adderall의 레보암페타민 성분은 덱스트로암페타민 단독에 비해 일부 개인들의 치료 반응을 향상시키는 것으로 보고되었습니다.애더럴의 유효 성분인 암페타민은 인간 미량 아민, 특히 암페타민의 [sources 2]위치 이성질체인 페네틸아민 및 N-메틸페닐아민과 많은 화학적 및 약리학적 특성을 공유합니다.2020년 애더럴은 2,600만 건 이상의 [31][32]처방을 받아 미국에서 22번째로 많이 처방된 약물이었습니다.
사용하다
의료의
애더럴은 주의력결핍 과잉행동장애(ADHD)와 기면증(수면장애)[33][13]을 치료하는 데 흔히 사용됩니다.일부 동물 종에서 충분히 고용량으로 암페타민에 장기간 노출되면 도파민 계통의 비정상적인 발달이나 신경 [34][35]손상이 발생하는 것으로 알려져 있지만 ADHD를 앓고 있는 사람의 경우 치료 용량으로 의약품 암페타민을 장기간 사용하면 뇌 발달과 신경 [36][37][38]성장이 개선되는 것으로 나타납니다.자기공명영상(MRI) 연구 리뷰에 따르면 암페타민을 장기간 투여하면 ADHD 환자의 뇌 구조와 기능의 이상이 감소하고, 기저신경절의 [36][37][38]우측 미상핵 등 뇌의 여러 부분의 기능이 개선되는 것으로 나타났습니다.
임상적 자극제 연구에 대한 검토는 ADHD [39][40][41]치료를 위한 암페타민 장기 지속 사용의 안전성과 효과를 확립했습니다.ADHD 치료를 위한 지속적인 자극제 치료의 무작위 대조 실험은 2년에 걸쳐 치료 효과와 [39][40]안전성을 입증했습니다.두 가지 리뷰는 ADHD에 대한 장기간의 지속적인 자극제 치료가 ADHD의 핵심 증상(즉, 과잉행동, 부주의, 충동성)을 감소시키고 삶의 질과 학업 성취도를 향상시키며 다음과 관련된 9개 범주의 결과에 걸쳐 많은 수의 기능적[note 3] 결과를 개선하는 데 효과적이라는 것을 나타냈습니다.학업, 반사회적 행동, 운전, 비흡연 약물 사용, 비만, 직업, 자존감, 서비스 사용(즉, 학업, 직업, 보건, 금융, 법률 서비스), 그리고 사회적 기능.[39][41]한 리뷰는 아이들을 대상으로 한 ADHD 암페타민 치료의 9개월 무작위 대조군 실험에서 평균 4.5 IQ 포인트 증가, 주의 집중력 지속 증가, 그리고 파괴적인 행동과 [40]과잉 행동의 지속적인 감소를 발견한 것을 강조했습니다.또 다른 리뷰는, 지금까지 수행된 가장 긴 추적 연구에 근거하여, 아동기에 시작되는 평생 자극제 치료가 ADHD 증상을 조절하는 데 지속적으로 효과적이며,[39] 성인이 되어서 물질 사용 장애가 발생할 위험을 감소시킨다는 것을 나타냈습니다.
ADHD의 현재 모델은 그것이 뇌의 신경전달물질 시스템 [23]중 일부의 기능적 장애와 관련이 있음을 시사합니다. 이러한 기능적 장애는 중피질콜림빅 투영에서의 도파민 신경전달 장애와 노르에피네프린 신경전달 장애를 수반합니다.피질[23]메틸페니데이트나 암페타민과 같은 정신자극제는 [14][23][42]이러한 시스템에서 신경전달물질의 활성을 증가시키기 때문에 ADHD 치료에 효과적입니다.이러한 자극제를 사용하는 사람들의 약 80%가 ADHD [43]증상의 개선을 봅니다.각성제를 사용하는 ADHD 어린이들은 일반적으로 또래나 가족들과 더 좋은 관계를 맺고, 학교 생활을 더 잘하며, 덜 산만하고 충동적이며, 주의 집중 [44][45]기간이 더 깁니다.제약 암페타민을 복용한 어린이, 청소년, 성인의 ADHD 치료에 대한 코크란[note 4] 리뷰는 단기 연구에서 이러한 약물이 증상의 심각성을 감소시킨다는 것을 증명했지만 부작용으로 인해 [47][48]비자극제보다 중단률이 높다고 밝혔습니다.투렛 증후군과 같은 틱 장애를 가진 아이들의 ADHD 치료에 대한 Cochrane 리뷰는 일반적으로 자극제가 틱을 더 악화시키지는 않지만, 덱스트로암페타민을 고용량 복용하면 일부 [49]사람들에서 틱을 악화시킬 수 있다고 밝혔습니다.
사용가능양식
Adderall은 IR(즉시 릴리스) 정제 또는 두 가지 다른 확장 릴리스([13][50]XR) 제제로 사용할 수 있습니다.확장 방출 캡슐은 일반적으로 [51]아침에 사용됩니다.더 짧은 12시간 연장 방출 제형은 애더럴 XR 브랜드로 출시되며, 치료 효과와 혈장 농도가 4시간 [50]간격으로 2회 투여하는 것과 동일하도록 설계되었습니다.16시간 동안 승인된 더 긴 확장 릴리스 제형은 마이다이스(Mydayis)라는 브랜드로 제공됩니다.미국에서는 Adderall의 즉시 방출 제제와 확장 방출 제제를 모두 제네릭 [52][53]의약품으로 사용할 수 있습니다.
성능향상
인지능력
2015년, 체계적인 검토와 고품질 임상 시험의 메타 분석에 따르면 암페타민은 낮은 (치료적) 용량으로 사용될 때 작업 기억, 장기적인 에피소드 기억, 억제 조절 및 주의의 일부 측면을 포함한 인지에서 완만하지만 명확한 개선을 생성한다고 합니다.정상적인 건강한 [54][55]성인에서; 암페타민의 이러한 인지력 향상 효과는 전전두엽 [14][54]피질에서 도파민 수용체1 D와 아드레노 수용체2 α의 간접적인 활성화를 통해 부분적으로 매개되는 것으로 알려져 있습니다.2014년부터 체계적으로 검토한 결과, 낮은 용량의 암페타민이 메모리 통합을 향상시켜 정보 [56]회수를 개선하는 것으로 나타났습니다.암페타민의 치료 용량은 또한 피질 네트워크 효율성을 향상시키는데, 이것은 모든 [14][57]개인의 작업 기억력의 향상을 중재하는 효과입니다.암페타민과 다른 ADHD 자극제는 또한 과제 현저성(과제를 수행하려는 동기)을 향상시키고 각성(깨어있음)을 증가시켜 목표 지향적인 [14][58][59]행동을 촉진합니다.암페타민과 같은 자극제는 어렵고 지루한 일들의 수행력을 향상시킬 수 있고 일부 학생들은 학습과 시험 [14][59][60]보는 보조제로 사용됩니다.대학생의 5~35%는 자가보고식 불법자극제 사용에 대한 연구를 통해 오락용 [61][62][63]약물보다는 학업성취도 향상을 위해 주로 사용되는 우회형 ADHD 자극제를 사용하는 것으로 나타났습니다.그러나 암페타민 용량이 치료 범위를 초과하면 작업 기억과 인지 [14][59]조절의 다른 측면을 방해할 수 있습니다.
물리적 성능
암페타민은 지구력과 [15][27]경각심을 증가시키는 것과 같은 심리적 그리고 운동 경기력 향상 효과를 위해 일부 운동선수들에 의해 사용되지만, 비의료용 암페타민 사용은 대학, 국내 그리고 국제 도핑 방지 [64][65]기관에 의해 규제되는 스포츠 경기에서 금지됩니다.경구 치료 용량의 건강한 사람에서 암페타민은 반응 [15][66][67]시간을 향상시키면서 근력, 가속도, 혐기성 조건에서의 운동 능력 및 지구력을 향상시키는 것으로 나타났습니다.암페타민은 주로 중추신경계에서 [66][67][68]도파민의 재흡수 억제와 방출을 통해 지구력과 반응 시간을 향상시킵니다.암페타민 및 기타 도파민 작용 약물은 또한 "안전 스위치"를 우선함으로써 고정된 수준의 운동에서 출력을 증가시켜 코어 온도 한계를 증가시켜 일반적으로 [67][69][70]사용할 수 없는 예비 용량에 접근할 수 있습니다.치료 용량에서 암페타민의 부작용은 운동 [15][66]수행을 방해하지 않지만 훨씬 더 많은 용량에서 암페타민은 급격한 근육 파괴와 체온 [16][66]상승과 같은 수행 능력을 심각하게 손상시키는 효과를 유발할 수 있습니다.
애더럴은 미국프로풋볼리그(NFL), 메이저리그(MLB), 미국프로농구(NBA), 미국대학육상협회(NCAA)[71]에서 출전이 금지됐습니다.NFL과 같은 리그에서는 운동선수가 [71]의사로부터 약물을 의학적으로 처방받았을 때에도 이 규칙에 대한 면제를 받기 위해 매우 엄격한 절차가 요구됩니다.
오락의
애더럴은 오락용 [72][73][74]약물로 오용될 가능성이 높습니다.애더럴 정제는 삼키거나, 으깨어 코를 들이마시거나, 물에 녹여서 [75]주입할 수 있습니다.정제 안에 있는 불용성 필러가 작은 [75]혈관을 막을 수 있기 때문에 혈류로 주사하는 것은 위험할 수 있습니다.
중등학교 이후의 많은 학생들은 선진국의 [74]여러 지역에서 공부 목적으로 애더럴을 사용한다고 보고했습니다.이 학생들 중 ADHD 자극제를 오락적으로 오용하는 위험 요소들 중 일부는 다음을 포함합니다: 일탈적 성격 특성을 소유하는 것(즉, 비행 또는 일탈 행동을 보이는 것), 부적절한 장애 수용, 외적 타당성에 근거한 자신의 가치, 낮은 자기 효능감, 낮은 성적,치료받지 않은 정신 건강 [74]장애를 가지고 있을 겁니다
금기사항
역효과
Adderall의 부작용은 다양하고 다양하지만,[16][27] 부작용의 가능성과 심각성을 결정하는 주요 요인은 소비되는 물질의 양입니다.Adderall은 현재 미국 [16]식품의약국에 의해 장기간의 치료적 사용을 승인받았습니다. Adderall의 오락적 사용은 일반적으로 훨씬 더 많은 용량을 포함하므로 치료 [27]목적으로 사용되는 용량보다 훨씬 더 큰 심각한 약물 부작용의 위험을 수반하는 훨씬 더 위험합니다.
물리적.
심혈관 부작용으로는 혈관 반응으로 인한 고혈압이나 저혈압, 레이노 현상(손과 발의 혈류량 감소), 빈맥(심장 [16][27][86]박동수 증가) 등이 있습니다.남성의 성적 부작용으로는 발기부전, 잦은 발기, 장시간 [16]발기 등이 있을 수 있습니다.위장관 부작용으로는 복통, 변비, 설사,[7][16][87] 메스꺼움 등이 있을 수 있습니다.다른 잠재적인 신체적 부작용으로는 식욕 감퇴, 흐릿한 시력, 마른 입, 과도한 치아 갈기, 코피, 심한 땀 흘리기, 비염 약독증(약물로 인한 코막힘), 발작 역치 감소, 틱(움직임의 일종), 체중 감소 [sources 3]등이 있습니다.위험한 신체적 부작용은 일반적인 약제학적 [27]용량에서는 거의 발생하지 않습니다.
암페타민은 정수리 호흡기 중추를 자극해 더 빠르고 깊은 [27]호흡을 만들어냅니다.치료 용량을 투여하는 정상인의 경우, 이러한 효과는 보통 눈에 띄지 않지만, 이미 호흡이 손상되었을 때,[27] 명백할 수 있습니다.암페타민은 소변을 조절하는 근육인 요광 괄약근에도 수축을 유도해 [27]소변을 보는 데 어려움을 겪을 수 있습니다.이 효과는 침구 습윤과 방광 [27]조절 상실을 치료하는 데 유용할 수 있습니다.암페타민이 위장관에 미치는 영향은 예측할 [27]수 없습니다.장 활동이 왕성한 경우 암페타민은 위장 운동성(내용물이 소화기관을 통해 이동하는 속도)[27]을 감소시킬 수 있지만, 트랙의 평활근이 [27]이완되면 암페타민은 운동성을 증가시킬 수 있습니다.암페타민은 또한 약간의 진통 효과가 있고 [7][27]오피오이드의 통증 완화 효과를 강화시킬 수 있습니다.
2011년 미국 식품의약국이 의뢰한 연구에 따르면 어린이, 청소년 및 성인의 경우 심각한 심혈관 질환(급사, 심장마비, 뇌졸중)과 암페타민 또는 기타 ADHD 자극제의 [sources 4]의학적 사용 사이에 연관성이 없는 것으로 나타났습니다.그러나 암페타민 제제는 심혈관 [sources 5]질환을 가진 사람에게는 사용할 수 없습니다.
심리학적
정상적인 치료 용량에서 암페타민의 가장 일반적인 심리적 부작용은 경각심, 불안, 집중력, 주도성, 자신감과 사교성 증가, 기분 변화(기분이 약간 우울한 기분이 뒤따르는 흥분), 불면증이나 각성, [16][27]피로감 감소 등입니다.덜 일반적인 부작용으로는 불안, 성욕의 변화, 거창함, 짜증, 반복적이거나 강박적인 행동, 그리고 [sources 6]안절부절못하는 것 등이 있습니다. 이러한 영향은 사용자의 성격과 현재 정신 [27]상태에 따라 달라집니다.암페타민 정신병(예: 망상과 편집증)은 심한 [16][17][95]사용자에게서 발생할 수 있습니다.매우 드물지만, 이 정신병은 장기간 치료 [16][95][18]중에 치료 용량으로도 발생할 수 있습니다.미국 식품의약국에 따르면 자극제가 공격적인 행동이나 [16]적대감을 유발한다는 "체계적인 증거는 없다"고 합니다.
암페타민은 또한 치료 [47][96]용량을 복용하는 사람들에게서 조건부 장소 선호도를 생성하는 것으로 나타났는데, 이는 개인들이 이전에 [96][97]암페타민을 사용했던 장소에서 시간을 보내는 선호도를 얻는다는 것을 의미합니다.
보강장애
중독
| 중독 및 의존 용어집[97][98][99] | |
|---|---|
| |
| 전사인자용어사전 | |
|---|---|
| |
중독은 오락용 암페타민을 많이 사용할 경우 심각한 위험이지만, 치료 [39][19][20]용량으로 장기간의 의학적 사용으로 발생할 가능성은 거의 없습니다. 사실, ADHD에 대한 평생 자극제 치료는 [39]성인이 되어서 물질 사용 장애가 발생할 위험을 줄여줍니다.복측 부위와 핵 침적을 연결하는 도파민 경로인 중절임빅 경로의 병리학적 과잉 활성화는 암페타민 [107][108]중독의 중심 역할을 합니다.암페타민을 고용량으로 자주 자가 투여하는 사람들은 만성적인 고용량 사용으로 중독에 대한 "분자 스위치" 및 [98][109][110]"마스터 컨트롤 단백질"인 축적된 ΔFosB의 수치가 점차 증가하기 때문에 암페타민 중독에 걸릴 위험이 높습니다.일단 핵이 축적되면 ΔFosB가 충분히 과발현되면,[109][111] 그것은 그 발현이 더 증가하면서 중독 행동의 심각성(즉, 강박적 약물 추구)을 증가시키기 시작합니다.현재 암페타민 중독을 치료할 수 있는 효과적인 약이 없지만, 규칙적으로 지속적인 유산소 운동을 하는 것이 그러한 [112][113]중독의 위험을 줄이는 것으로 보입니다.운동 요법은 임상적 치료 결과를 향상시키고 [112][114][sources 7]중독에 대한 행동 요법과 함께 보조 요법으로 사용될 수 있습니다.
생체분자기전
암페타민을 과도한 용량으로 만성적으로 사용하는 것은 전사 [110][115][116]및 후성유전학적 메커니즘을 통해 발생하는 중피질자극술의 유전자 발현 변화를 야기합니다.이러한 변화를 일으키는 가장 중요한 전사[note 8] 인자는 델타 FBJ 뮤린 골육종 바이러스 종양 유전자 상동성 B (ΔFosB), cAMP 반응 요소 결합 단백질 (CREB), 핵인자-카파 B (NF-κB)[110]입니다.ΔFosB는 중독에서 가장 중요한 생체 분자 메커니즘입니다. 왜냐하면 ΔFosB 과발현(즉, 뚜렷한 유전자 관련 표현형을 생성하는 비정상적으로 높은 수준의 유전자 발현)은 신경 적응의 많은 부분에 필요하고[note 9] 충분하며 다중 행동을 조절하기 때문입니다.중독과 [98][109][110]관련된 바이러스 효과(예: 보상 감작 및 약물 자가 투여 증가)일단 ΔFosB가 충분히 과발현되면, 그것은 ΔFosB [98][109]발현이 더 증가함에 따라 점점 더 심해지는 중독 상태를 유도합니다.그것은 알코올, 칸나비노이드, 코카인, 메틸페니데이트, 니코틴, 오피오이드, 펜시클리딘, 프로포폴,[sources 8] 치환된 암페타민 등에 대한 중독과 관련되어 있습니다.
전사인자인 ΔJunD와 히스톤 메틸트랜스퍼라제 효소인 G9a는 모두 ΔFosB의 기능을 억제하고 발현 [98][110][120]증가를 억제합니다.바이러스 벡터와 함께 핵에 있는 ΔJunD를 충분히 과발현하면 만성 약물 남용에서 볼 수 있는 많은 신경 및 행동 변화(즉, [110]ΔFosB에 의해 매개되는 변화)를 완전히 차단할 수 있습니다.유사하게, 축적된 G9a 과발현은 현저하게 증가된 히스톤 3 라이신 잔기 9 디메틸화(H3K9me2)를 초래하고,[sources 9] 만성 약물 사용에 의한 ΔFosB-매개 신경 및 행동 가소성의 유도를 차단하며, 이는 다양한 ΔFosB 및 H3K9me2의 전사 인자의 H3K9me2-매개 억제를 통해 발생합니다.전사 대상 (예를 들어 CDK5).[110][120][121] ΔFosB는 또한 입맛에 맞는 음식, 성별, [111][110][124]운동과 같은 자연적 보상에 대한 행동적 반응을 조절하는 데 중요한 역할을 합니다.자연적 보상과 중독 약물 모두 ΔFosB의 발현을 유도하기 때문에(즉, 뇌가 더 많은 양을 생산하도록 한다), 이러한 보상의 만성적인 획득은 유사한 병적 중독 [111][110]상태를 초래할 수 있습니다.결과적으로 ΔFosB는 암페타민 중독과 암페타민 과다 [111][125][126]복용으로 인한 강박적인 성행위인 암페타민 중독과 암페타민 유발 성중독 모두에 가장 중요한 요인으로 작용하고 있습니다.이러한 성적 중독은 도파민제를 [111][124]복용하는 일부 환자들에게 나타나는 도파민 조절 장애 증후군과 관련이 있습니다.
암페타민이 유전자 조절에 미치는 영향은 용량과 경로 모두에 [116]의존적입니다.유전자 조절과 중독에 대한 연구의 대부분은 매우 높은 [116]용량의 정맥내 암페타민 투여를 통한 동물 연구에 근거하고 있습니다.동등한 (중량 조정된) 인체 치료 용량과 경구 투여를 사용한 소수의 연구는 이러한 변화가 발생한다면 상대적으로 [116]미미하다는 것을 보여줍니다.이는 암페타민의 의학적 사용이 유전자 [116]조절에 큰 영향을 미치지 않는다는 것을 시사합니다.
약리학적 치료
2019년 [update]12월 현재 암페타민 [127][128][129]중독에 대한 효과적인 약물치료는 없습니다.2015년과 2016년의 리뷰에 따르면 TAAR1 선택적 작용제는 정신자극제 [130][131]중독의 치료제로서 상당한 치료 가능성을 가지고 있지만,[update] 2016년 2월 현재 TAAR1 선택적 작용제로서 기능하는 것으로 알려진 유일한 화합물은 실험 [130][131]약물입니다.암페타민 중독은 주로 도파민 수용체의 증가된 활성화와 핵 내의 공국적 NMDA[note 10] 수용체의 [108]축적을 통해 매개됩니다; 마그네슘 이온은 수용체 칼슘 [108][132]채널을 차단함으로써 NMDA 수용체를 억제합니다.한 리뷰는 동물 실험에 근거하여, 병리학적 (중독 유발) 심리 자극제 사용이 [108]뇌 전체에 걸쳐 세포 내 마그네슘의 수준을 상당히 감소시킨다고 제안했습니다.마그네슘[note 11] 보충 치료는 인간의 암페타민 자가 투여(즉, 자신에게 투여되는 용량)를 감소시키는 것으로 나타났지만, 암페타민 [108]중독에 대한 효과적인 단독 치료는 아닙니다.
2019년 체계적인 검토 및 메타 분석을 통해 암페타민 및 필로폰 [128]중독에 대한 무작위 대조군 시험(RCT)에 사용되는 17가지 약물 치료법의 효과를 평가했습니다. 메틸페니데이트가 암페타민 또는 필로폰 자가 [128]투여를 감소시킬 수 있다는 저강도 증거만 발견했습니다.항우울제(부프로피온, 미르타자핀, 서트랄린), 항정신병약(아리피프라졸), 항경련제(토피라메이트, 바클로펜, 가바펜틴), 날트렉손, 바레니클린, 씨티콜린, 온단세트론, 프로메타, 릴루졸, 아토목세틴, 덱스트로아 등 RCT에 사용된 대부분의 다른 약물에 대해 저강도에서 중간 강도의 증거가 있었습니다.음페타민과 [128]모다피닐이요
행동치료
암페타민, 필로폰 또는 코카인 중독에 대한 12가지 다른 심리 사회적 개입을 포함한 50개 실험의 2018년 체계적 검토 및 네트워크 메타 분석에 따르면 우연성 관리 및 지역 사회 강화 접근 방식을 모두 포함한 조합 치료가 가장 높은 효과(즉, 절주율)와 수용성(즉,)을 가진 것으로 나타났습니다.가장 낮은 탈락률).[133]분석에서 분석된 다른 치료 양식에는 우연성 관리 또는 공동체 강화 접근법을 사용한 단일 요법, 인지 행동 치료, 12단계 프로그램, 비일관적 보상 기반 치료, 정신 역학 치료 및 [133]이와 관련된 다른 조합 치료가 포함되었습니다.
또한, 신체 운동의 신경생물학적 효과에 대한 연구는 일상 유산소 운동, 특히 지구력 운동(마라톤 달리기)이 약물 중독의 발생을 방지하고 암페타민 [sources 7]중독에 대한 효과적인 보조 치료(즉, 보충 치료)임을 시사하고 있습니다.운동은 특히 정신 자극 중독에 대한 보조 치료로 사용될 [112][114][134]때 더 나은 치료 결과로 이어집니다.특히, 유산소 운동은 정신 자극 자가 투여를 감소시키고, 약물 추구의 복원(즉, 재발)을 감소시키며,[111][134] 선조체에서 증가된 도파민 수용체2 D(DRD2) 밀도를 유도합니다.이것은 병리학적 자극제의 사용과는 반대로, 선조체 DRD2 [111]밀도의 감소를 유도합니다.한 리뷰는 운동이 선조체 또는 보상 [113]시스템의 다른 부분에서 ΔFosB 또는 c-Fos 면역 반응을 변경함으로써 약물 중독의 발생을 방지할 수 있다고 언급했습니다.
| 신경가소성의 형태 또는 행동 가소성 | 보강재 종류 | 원천 | |||||
|---|---|---|---|---|---|---|---|
| 아편스 | 심리자극제 | 고지방 또는 당분이 많은 식품 | 성관계 | 운동 (주로) | 환경의 농축. | ||
| ΔFosB 표현식의 핵이 쌓이다D1형MSNs툴팁 배지 가시 뉴런 | ↑ | ↑ | ↑ | ↑ | ↑ | ↑ | [111] |
| 행동 가소성 | |||||||
| 흡입구 에스컬레이션 | 네. | 네. | 네. | [111] | |||
| 심리자극제 교차 감응 | 네. | 해당없음 | 네. | 네. | 감쇄된 | 감쇄된 | [111] |
| 심리자극제 자치의 | ↑ | ↑ | ↓ | ↓ | ↓ | [111] | |
| 심리자극제 조건부 장소 선호도 | ↑ | ↑ | ↓ | ↑ | ↓ | ↑ | [111] |
| 마약 추구 행위의 복직 | ↑ | ↑ | ↓ | ↓ | [111] | ||
| 신경화학적 가소성 | |||||||
| CREB툴팁 cAMP반응요소결합단백질 인산화 핵에 침잠하여 | ↓ | ↓ | ↓ | ↓ | ↓ | [111] | |
| 감작된 도파민 반응 핵에 침잠하여 | 아니요. | 네. | 아니요. | 네. | [111] | ||
| 변화된 선조체 도파민 신호전달 | ↓DRD2, ↑DRD3 | ↑DRD1, ↓DRD2, ↑DRD3 | ↑DRD1, ↓DRD2, ↑DRD3 | ↑DRD2 | ↑DRD2 | [111] | |
| 변화된 선조체 오피오이드 신호전달 | 잔돈 없음 또는 ↑μ-아미노산 수용체 | ↑μ-아미노산 수용체 ↑아미노-아미노산 수용체 | ↑μ-아미노산 수용체 | ↑μ-아미노산 수용체 | 잔돈 없음 | 잔돈 없음 | [111] |
| 선조체 오피오이드 펩타이드의 변화 | ↑디노르핀 변경사항 없음: 엔케팔린 | ↑디노르핀 | ↓엔케팔린 | ↑디노르핀 | ↑디노르핀 | [111] | |
| 중피질임부 시냅스 가소성 | |||||||
| 핵내 수지상 조직의 수 | ↓ | ↑ | ↑ | [111] | |||
| 수지상 척추밀도는 핵이 쌓이다 | ↓ | ↑ | ↑ | [111] | |||
의존 및 인출
약물 내성은 암페타민 남용(즉, 오락용 암페타민 사용)에서 빠르게 발생하므로, 연장 남용 기간에는 동일한 효과를 [135][136]달성하기 위해 점점 더 많은 양의 약물이 필요합니다.암페타민과 필로폰을 강박적으로 복용하는 사람들의 금단현상에 대한 코크란 리뷰에 따르면 "만성 중환자가 갑자기 암페타민 복용을 중단하면 많은 사람들이 마지막 [137]복용 후 24시간 이내에 발생하는 시한부 금단증후군을 보고한다"고 합니다.이 리뷰는 만성 고용량 사용자의 금단 증상이 약 88%의 사례에서 자주 발생하며, 첫 주 [137]동안 현저한 "충돌" 단계와 함께 3-4주 동안 지속된다는 점에 주목했습니다.암페타민 금단 증상에는 불안, 약물 갈망, 우울한 기분, 피로, 식욕 증가, 움직임 증가 또는 감소, 동기 부족, 불면증 또는 졸림,[137] 자각몽 등이 포함될 수 있습니다.검토 결과, 금단증상의 심각성은 개인의 연령 [137]및 의존 정도와 긍정적인 상관관계가 있는 것으로 나타났습니다.암페타민 치료의 중단으로 인한 가벼운 금단 증상은 치료 용량을 [7]줄이면 피할 수 있습니다.
과다 복용
암페타민 과다 복용은 많은 다양한 증상을 초래할 수 있지만 적절한 [138][80][139]관리로 치명적인 경우는 거의 없습니다.과다복용 증상의 심각성은 용량에 따라 증가하고 [140][80]암페타민에 대한 약물 내성에 따라 감소합니다.내성이 있는 사람들은 하루에 암페타민을 5그램이나 복용하는 것으로 알려져 있는데, 이는 하루 최대 치료 [80]용량의 약 100배에 달합니다.중등도 이상의 약물 과다 복용 증상은 아래에 나열되어 있습니다. 치명적인 암페타민 중독은 대개 경련과 혼수 상태를 [79][140]수반합니다.2013년 암페타민, 필로폰 및 "암페타민 사용 장애"와 관련된 기타 화합물의 과다 복용으로 인해 전 세계적으로 약 3,788명이 사망했습니다(3,425–4,145명 사망, 95% 신뢰).[note 12][141]
| 시스템. | 경미하거나 중등도의[79][140][80] 과다복용 | 심한[sources 10] 과다복용 |
|---|---|---|
| 심혈관의 | ||
| 중추신경계 시스템. |
| |
| 근골격계 |
| |
| 호흡기 |
| |
| 비뇨기 | ||
| 다른. |
상호작용
- 암페타민과 함께 복용하는 모노아민 산화효소 억제제(MAOIs)는 MAOI 타입의 [144]약물을 마지막으로 사용한 후 2주 이내에 복용할 경우 고혈압 위기를 초래할 수 있습니다.
- 암페타민을 직접 대사하는 효소(특히 CYP2D6 및 FMO3)의 억제제는 암페타민의 제거를 연장시키고 약물 [144][145][146]효과를 증가시킬 것입니다.
- 암페타민과 병용 투여하는 세로토닌계 약물(대부분의 항우울제 등)은 세로토닌 [146]증후군의 위험을 증가시킵니다.
- 자극제와 항우울제(진정제와 우울제)는 암페타민의 약물 효과를 증가(감소)시킬 수 있고,[144] 그 반대도 마찬가지입니다.
- 위장관과 요중 pH는 각각 암페타민의 흡수와 제거에 영향을 미칩니다.위장관 알칼리화제는 암페타민의 흡수를 증가시킵니다.요알칼리화제는 비이온화된 종의 농도를 증가시켜 요 [144]배설을 감소시킵니다.
- 프로톤-펌프 억제제(PPIs)는 Adderall XR과 Mydayis의 [144][146]흡수를 조절합니다.
- 아연 보충제는 암페타민이 [note 13][150]ADHD 치료에 사용될 때 암페타민의 최소 유효 용량을 감소시킬 수 있습니다.
약리학
도파민 뉴런의 암페타민 약동역학 |
작용기전
애더럴의 유효성분인 암페타민은 주로 [23][42]뇌에서 신경전달물질인 도파민과 노르에피네프린의 활성을 증가시켜 작용합니다.또한, 특정 신경펩타이드(예를 들어 코카인 및 암페타민 조절 전사체([25][156]CART) 펩타이드)의 합성뿐만 아니라 여러 다른 호르몬(예를 들어, 에피네프린) 및 신경전달물질(예를 들어, 세로토닌 및 히스타민)의 방출을 유발합니다.애더럴의 활성 성분인 덱스트로암페타민과 레보암페타민은 동일한 생물학적 [27][28]표적에 결합하지만, 결합 친화성(즉, 효력)은 [27][28]다소 다릅니다.덱스트로암페타민 및 레보암페타민은 둘 다 미량 아민 연관 수용체 1(TAAR1)의 강력한 완전 작용제(활성화 화합물)이며, 소포체 모노아민 수송체 2(VMAT2)와 상호 작용하며, 덱스트로암페타민은 TAAR1의 [28]더 강력한 작용제입니다.결과적으로 덱스트로암페타민은 [28][157]레보암페타민보다 더 많은 자극을 주지만, 레보암페타민은 심혈관 및 말초 [27]효과가 약간 더 큽니다.특정 어린이들이 [29][30]레보암페타민에 대해 더 나은 임상 반응을 보인다고 보고되었습니다.
암페타민이 없을 경우, 일반적으로 모노아민(예: 도파민, 히스타민, 세로토닌, 노르에피네프린 등)을 모노아민 뉴런의 세포 내 유체에서 시냅스 소포로 이동시켜 나중에 방출하기 위한 신경 전달 물질을 시냅스 [25]분열로 저장합니다.암페타민이 뉴런으로 들어가 VMAT2와 상호작용하면, 운반자는 운반 방향을 반대로 하여 시냅스 소포 안에 저장된 모노아민을 뉴런의 세포 내 [25]유체로 다시 방출합니다.한편, 암페타민이 활성화될 때, 수용체는 뉴런의 세포막 결합 모노아민 수송체(즉, 도파민 수송체, 노르에피네프린 수송체, 또는 세로토닌 수송체)가 모노아민의 수송을 완전히 중단하거나(수송체 내재화를 통해) [24]뉴런 밖으로 모노아민을 수송하게 합니다; 즉,역전된 막 수송체는 도파민, 노르에피네프린, 세로토닌을 뉴런의 세포내 유체에서 시냅스의 [24]분열로 밀어냅니다.요약하면, 암페타민은 VMAT2 및 TAAR1 둘 다와 상호작용함으로써 시냅스 소포에서 신경 전달 물질을 세포 내 유체로 방출하고, 이후 막 결합된 역전 모노아민 전달체(TAAR1 [24][25]효과)를 통해 뉴런을 빠져나갑니다.
약동학
암페타민의 경구 생체 이용률은 위장관 [16]pH에 따라 다양하며; 장내에서 잘 흡수되며, 덱스트로암페타민의 [158]경우 생체 이용률은 일반적으로 75% 이상입니다.암페타민은 pK가a 9.[159]9인 약한 염기입니다; 결과적으로, pH가 염기성일 때, 더 많은 약물이 지질 용해성 유리 염기 형태에 있고, 더 많은 약물이 내장 [159][16]상피의 지질이 풍부한 세포막을 통해 흡수됩니다.반대로, 산성 pH는 약물이 주로 수용성 양이온(염) 형태이고 [159]흡수가 적다는 것을 의미합니다.혈류에서 순환하는 암페타민의 약 20%가 혈장 [160]단백질과 결합되어 있습니다.암페타민은 흡수 후 체내 대부분의 조직에 쉽게 분포하며, 뇌척수액과 [161]뇌조직에서 고농도로 발생합니다.
암페타민계 항산제의 반감기는 소변 [159]pH에 따라 다르고 다릅니다.정상적인 소변 pH에서 덱스트로암페타민과 레보암페타민의 반감기는 각각 [159]9-11시간과 11-14시간입니다.고도로 산성화된 소변은 에난티오머 [161]반감기를 7시간으로 감소시킬 것이고, 고도로 알칼리화된 소변은 반감기를 [161]34시간까지 증가시킬 것입니다.두 이성질체의 염의 즉시 방출 및 확장 방출 변형은 투여 후 각각 [159]3시간 및 7시간에서 최고 혈장 농도에 도달합니다.암페타민은 신장을 통해 제거되며, 정상적인 소변 [159]pH에서 약물의 30-40%가 변하지 않고 배출됩니다.요로 pH가 기본인 경우 암페타민은 유리염기 형태이므로 배설량이 [159]적습니다.소변 pH가 비정상적인 경우 암페타민의 소변 회수율은 [159]1%대에서 75%대까지 다양할 수 있으며, 이는 소변이 너무 기초적인지 산성적인지에 따라 주로 좌우됩니다.경구 투여 후 3시간 이내에 소변에서 [161]암페타민이 검출됩니다.섭취한 암페타민의 약 90%는 마지막 경구 [161]투여 3일 후에 제거됩니다.
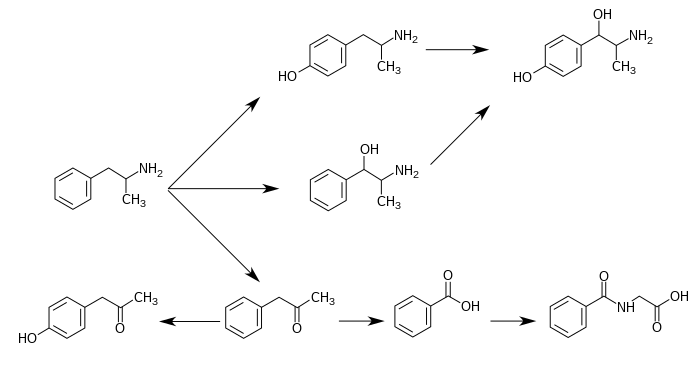
CYP2D6, 도파민 β-하이드록실라아제(DBH), 플라빈 함유 모노옥시게나아제3(FMO3), 부틸레이트-CoA 리가아제(XM-리가아제) 및 글리신 N-아실트랜스퍼라아제(GLYAT)는 암페타민 또는 이의 대사물을 [sources 11]인간에서 대사하는 것으로 알려진 효소.암페타민은 4-하이드록시암페타민, 4-하이드록시노레페드린, 4-하이드록시페닐아세톤,[159][162] 벤조산, 히푸릭산, 노레페드린 및 페닐아세톤을 포함한 다양한 배설 대사 생성물을 가지고 있습니다.이러한 대사 물질들 중에서, 활성 공감모방제는 4-하이드록시암페타민,[163] 4-하이드록시노레페드린 [164][165]및 노레페드린입니다.주요 대사 경로는 방향족 파라하이드록실화, 지방족 알파 및 베타하이드록실화, N-산화, N-탈알킬화 및 탈아민화를 [159][166]포함합니다.알려진 대사 경로, 검출 가능한 대사 물질 및 인간의 대사 효소는 다음과 같습니다.
약미생물학
인간 메타게놈(즉, 한 개체의 유전적 구성과 그 개체의 몸 위 또는 몸 안에 존재하는 모든 미생물)은 [175][176]개체 간에 상당한 차이가 있습니다.인체 내 미생물 및 바이러스 세포의 총 수(100조 이상)가 인간 세포(수십조 [note 15][175][177]이상)를 크게 초과하기 때문에 약물과 개인의 마이크로바이옴 간의 상호 작용 가능성은 상당합니다. 다음을 포함하여 인간 마이크로바이옴의 구성을 변경하는 약물, 미생물 효소에 의한 약물 대사 modify.ng 약물의 약동학적 프로파일, 및 약물의 임상적 효능 및 [175][176][178]독성 프로파일에 영향을 미치는 미생물 약물 대사.이러한 상호작용을 연구하는 분야는 약미생물학으로 [175]알려져 있습니다.
암페타민은 대부분의 생체분자 및 다른 경구 투여된 제노바이오틱스(즉, 약물)와 유사하게 [178]혈류로 흡수되기 전에 인간 위장관 미생물(주로 박테리아)에 의해 난잡한 대사를 겪을 것으로 예측됩니다.2019년 [178]인간의 내장에서 흔히 발견되는 대장균 균주의 티라민 산화효소가 최초의 암페타민 대사 미생물 효소로 확인되었습니다.이 효소는 암페타민, 티라민 및 페네틸아민을 세 가지 [178]화합물 모두에 대해 거의 동일한 결합 친화도로 대사시키는 것으로 밝혀졌습니다.관련 내생성 화합물
암페타민은 인체와 [24][26][179]뇌에서 자연적으로 생성되는 신경조절물질인 내인성 미량아민과 매우 유사한 구조와 기능을 가지고 있습니다.이 그룹 중에서, 가장 밀접한 관련이 있는 화합물은 암페타민의 모 화합물인 페네틸아민과 암페타민의 이성질체인 N-메틸페네틸아민(즉, 분자식이 [24][26][180]동일함)입니다.인간에서 페네틸아민은 방향족 아미노산 탈카복실화효소(AADC)에 의해 L-페닐알라닌으로부터 직접적으로 생성되며, 이 효소는 [26][180]L-DOPA를 도파민으로 전환시키기도 합니다.결국, N-메틸페닐에틸아민은 페닐에틸아민으로부터 노르에피네프린을 [26][180]에피네프린으로 대사시키는 것과 동일한 효소인 페닐에탄올아민 N-메틸트랜스퍼라제에 의해 대사됩니다.암페타민과 마찬가지로 페네틸아민과 N-메틸페네틸아민 모두 모노아민 신경전달을 [24][179][180]조절합니다.[26][180] 암페타민과 달리 이들 물질은 모노아민 산화효소 B에 의해 분해되므로 암페타민보다 반감기가 짧습니다.
역사
제약사 렉사는 1973년 의약품 효능 연구 구현(DESI) 프로그램 결과로 인해 연방 식품·의약품·화장품법에 대한 케파우버 해리스 개정안에 따라 시장에서 의무적으로 철수한 후 인기 있는 체중 감량 의약품 오베트롤을 재구성했습니다.새로운 제제는 단순히 2개의 필로폰 성분을 같은 무게의 덱스트로암페타민과 암페타민 성분으로 대체하고(다른 2개의 오리지널 덱스트로암페타민과 암페타민 성분은 보존), 오베트롤 브랜드를 보존하고, FDA 승인을 받지 못했음에도 불구하고,그것은 여전히 시장에 출시되었고 수년동안 렉사에 의해 판매되고 팔렸습니다.
1994년, Richwood Pharmaceuticals는 Rexar를 인수하여 ADHD 치료제로서 오베트롤을 홍보하기 시작했고, 현재 Adderall이라는 새로운 브랜드 이름으로 판매되고 있으며, 이는 마케팅 [181]목적으로 "A.D.D. for All"이라는 문구를 의미하는 "A.D.D."라는 문구의 축약형입니다.FDA는 오베트롤과 관련된 수많은 중대한 CGMP 위반이 인수 후 정기적인 검사(위반에 대한 공식 경고장 발급 포함) 중에 발견되었다고 회사를 인용하였습니다.이후 리치우드 제약사에 "신약 및 FD&C 법의 잘못된 브랜드 규정" 위반으로 인해 구체적으로 두 번째 공식 경고 서한을 발표했습니다.회사의 수많은 FDA 규정 위반과 관련된 많은 문제를 해결하기 위해 리치우드 제약사와 오랜 논의 끝에 FDA는 공식적으로 첫 번째 오베트롤 라벨링을 승인했습니다.1996년 NDA 개정으로 Adderall로 이름을 변경하고 승인된 [182][183]의약품으로 지위를 회복하는 것을 포함합니다.1997년 리치우드 제약은 1억 8천 6백만 달러에 샤이어 제약에 인수되었습니다.[181]
나중에 Shire plc와 합병한 Richwood Pharmaceuticals는 1996년에 현재의 Adderall 브랜드를 즉시 출시 태블릿으로 [184]선보였습니다.2006년, 샤이어는 듀라메드 [185]제약사에 즉시 출시되는 형태의 의약품에 대한 애더럴 명칭에 대한 권리를 판매하기로 합의했습니다.DuraMed Pharmaceuticals는 Bar's Duramed [186]사업부를 포함한 Bar Pharmaceuticals를 인수하는 과정에서 2008년 Teva Pharmaceuticals에 인수되었습니다.
애더럴 IR의 첫 번째 제네릭 버전은 [9]2002년에 시장에 소개되었습니다.이후 바와 샤이어는 2009년 [9][187]4월부터 바가 확장 방출 약물의 일반적인 형태를 제공하는 것을 허용하는 합의에 도달했습니다.
상용제제
화학적으로, 애더럴은 4개의 암페타민 염의 혼합물입니다; 구체적으로, 그것은 동일한 양의 암페타민 아스파르트산 일수화물, 암페타민 황산염, 덱스트로암페타민 황산염, 그리고 덱스트로암페타민 [50]사카레이트로 구성됩니다.이 약물 혼합물은 덱스트로암페타민의 [24][27]비율이 높기 때문에 라세믹암페타민보다 약간 강한 효과를 가지고 있습니다.애더럴은 즉시 릴리스(IR) 및 확장 릴리스([9][13][50]XR) 제형으로 모두 생산됩니다.2013년 12월[update] 기준으로 제네릭 애더럴 IR은 10개 회사가 생산하고 있으며, 테바제약공업, 엑타비스, 바제약 등은 제네릭 애더럴 [9]XR을 생산하고 있습니다.2013년 현재[update] 애더럴 XR과 애더럴 XR의 원래 특허를 보유한 회사인 샤이어 plc는 브랜드명 애더럴 XR을 제조했지만 애더럴 [9]IR은 제조하지 않았습니다.
다른 제형과 비교
애더럴(Adderall)은 단일 또는 혼합 에난티오머 및 에난티오머 프로드러그를 포함하는 제약 암페타민의 여러 제형 중 하나입니다.아래 표는 미국 승인 양식을 기준으로 다음과 같은 의약품을 비교한 것입니다.
| 약물 | 공식 | 어금니 질량 [주 16] | 암페타민 염기 [주 17] | 암페타민 염기 같은 용량으로 | 로의 복용량. 등기저 내용을 [주 18] | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| (g/mol) | (퍼센트) | (30 mg 용량) | ||||||||
| 총 | 기초 | 총 | 덱스트로 | 레보의 | 덱스트로 | 레보의 | ||||
| 황산 덱스트로암페타민[189][190] | (C9H13N)2•H2SO4 | 368.49 | 270.41 | 73.38% | 73.38% | — | 22.0 mg | — | 30.0 mg | |
| 황산암페타민[191] | (C9H13N)2•H2SO4 | 368.49 | 270.41 | 73.38% | 36.69% | 36.69% | 11.0 mg | 11.0 mg | 30.0 mg | |
| 애더럴 | 62.57% | 47.49% | 15.08% | 14.2 mg | 4.5 mg | 35.2 mg | ||||
| 25% | 황산 덱스트로암페타민[189][190] | (C9H13N)2•H2SO4 | 368.49 | 270.41 | 73.38% | 73.38% | — | |||
| 25% | 황산암페타민[191] | (C9H13N)2•H2SO4 | 368.49 | 270.41 | 73.38% | 36.69% | 36.69% | |||
| 25% | 덱스트로암페타민 당산염[192] | (C9H13N)2•C6H10O8 | 480.55 | 270.41 | 56.27% | 56.27% | — | |||
| 25% | 아스파르트산 1수화물로서의[193] 암페타민 | (C9H13N)•C4H7NO4•H2O | 286.32 | 135.21 | 47.22% | 23.61% | 23.61% | |||
| 리스트샘페타민디메실레이트[194] | CHNO15253•(COS43)2 | 455.49 | 135.21 | 29.68% | 29.68% | — | 8.9mg | — | 74.2 mg | |
| 암페타민 베이스 현탁액[87] | C9H13N | 135.21 | 135.21 | 100% | 76.19% | 23.81% | 22.9mg | 7.1 mg | 22.0 mg | |
사회와 문화
법적지위
- 캐나다에서 암페타민은 통제 약물 및 물질법의 별표 I에 있으며 [195]처방전이 있어야만 얻을 수 있습니다.
- 일본에서는 암페타민이 함유된 의약품의 사용, 생산, 수입이 [196]금지되어 있습니다.
- 한국에서는 암페타민이 [197]금지되어 있습니다.
- 대만에서 애더럴을 포함한 암페타민은 최소 [198]5년 이상의 징역형을 받는 스케줄 2 약물입니다.리탈린만이 ADHD 치료를 위해 법적으로 처방될 수 있습니다.
- 태국에서 암페타민은 제1종 [199]마약으로 분류됩니다.
- 영국에서 암페타민은 B급 약물로 간주됩니다.무단 점유 시 최대 벌금은 징역 5년과 무제한 벌금입니다.부정 공급에 대한 최대 처벌은 징역 14년과 무제한 [200]벌금입니다.
- 미국에서 암페타민은 중추신경계([201]CNS) 자극제로 분류되는 스케줄 II 처방약입니다.
- 국제적으로 암페타민은 향정신성 [202][203]물질에 관한 협약의 별표 2에 있습니다.
부족함
2023년 2월, 뉴스 기관들은 5개월 [204][205]이상 지속된 미국의 애더럴 부족에 대해 보도하기 시작했습니다.식품의약품안전청은 2022년 [206]10월 처음으로 품귀 현상을 보고했습니다.부족한지 7개월이 지난 2023년 5월, 미국 식품의약국(FDA) 위원인 로버트 캘리프는 "수익이 충분하지 않기 때문에 많은 제네릭 의약품이 언제든지 부족하다"고 말했습니다.그는 애더럴이 통제된 물질이고 처방 가능한 양은 마약단속국이 통제하기 때문에 특별한 경우라고 지적합니다.그는 또한 가상 처방과 일반적인 과잉 처방 및 과잉 진단으로 인한 "처방의 엄청난 증가"를 탓하며 "이런 약이 필요한 사람들만 복용했다면 아마 [자극제][207][208] 부족은 없을 것"이라고 덧붙였습니다.
메모들
- ^ 라세믹 암페타민과 덱스트로암페타민의 염을 (1:1) 비율로 혼합하여 이 약을 생산합니다.레이스메이트는 동일한 부분의 덱스트로암페타민과 레보암페타민으로 구성되어 있기 때문에, 이 약물은 또한 암페타민의 D와 (L)-엔안티오머가 (3:1) 비율로 혼합된 것으로 설명될 수 있지만, 이 혼합물의 성분 중 어느 것도 레보암페타민 [1][2]염이 아닙니다.
- ^ 본 논문은 약물의 4염 조성물이 비독점적인 명칭(dextroampheton sulfate 25%, dextroampheton saccharate 25%, ampheton sulfate 25%, ampheton sulfate 25%, ampheton sulfate 25%, ampheton aspartate 25%)을 과도하게 [9]길게 하기 때문에 애더럴이라는 상호를 주로 사용하고 있음.My dayis는 일반적으로 [8]혼합물을 지칭하는 데 일반적으로 사용되지 않는 비교적 새로운 상호입니다.
- ^ 장기간 지속적인 각성제 치료로 현저하게 개선된 결과 중 가장 큰 비율을 차지하는 ADHD 관련 결과 영역에는 학업(학업적 결과의 55% 이상 개선됨), 운전(운전적 결과의 100% 개선됨), 비의료 약물 사용(중독 관련 결과의 47% 개선됨), 비만(비만 관련 결과의 65% 이상)이 포함됩니다.향상), 자아존중감(자존감 결과 50% 향상), 사회적 기능(사회적 기능 결과 67% 향상).[41]
장기적인 자극제 치료의 결과 개선을 위한 가장 큰 효과 크기는 학업(예: 성적 평균, 성취도 시험 점수, 교육 기간 및 교육 수준), 자아 존중감(예: 자아 존중감 설문 평가, 자살 시도 횟수 및 자살률), 사회적 기능(예: 사회적 기능)을 포함하는 영역에서 발생합니다.., 동료 지명 점수, 사회적 기술, 동료,[41] 가족, 연인 관계의 질).
ADHD에 대한 장기 복합 치료(즉, 자극제와 행동 치료를 모두 포함한 치료)는 장기 자극제 치료 [41]단독에 비해 결과 개선을 위해 훨씬 더 큰 효과 크기를 생성하고 각 영역에 걸쳐 더 많은 비율의 결과를 개선합니다. - ^ Cochrane 리뷰는 무작위 대조군 [46]시험에 대한 고품질 메타분석 체계적 리뷰입니다.
- ^ USFDA가 지지하는 진술은 정보를 처방할 때 나오는 것으로, 이것은 제조사의 저작권이 있는 지적 재산이며 USFDA가 승인한 것입니다. USFDA 금지는 반드시 의료행위를 제한하기 위한 것은 아니지만 제약회사의 [76]청구를 제한하기 위한 것입니다.
- ^ 한 리뷰에 따르면, 암페타민은 [77]처방 의사에게 매일 약물을 수령하도록 요구하는 등 적절한 약물 관리가 적용될 경우 남용 이력이 있는 사람에게 처방될 수 있습니다.
- ^ 정상 이하의 키와 체중 증가를 경험한 사람들은 자극제 치료가 잠시 [83][84][85]중단되면 정상 수준으로 회복될 것으로 예상됩니다.3년간의 지속적인 자극제 치료로 인한 최종 성인 키의 평균 감소량은 [85]2 cm입니다.
- ^ 전사인자는 특정 [117]유전자의 발현을 증가시키거나 감소시키는 단백질입니다.
- ^ 간단히 말하면, 이 필요충분한 관계는 핵에 있는 ΔFosB 과발현이 누적되고 중독과 관련된 행동 및 신경 적응이 항상 함께 일어나고 결코 혼자 일어나지 않는다는 것을 의미합니다.
- ^ NMDA 수용체는 전압에 의존하는 리간드 게이트 이온 채널로서 [132]이온 채널을 열기 위해 글루탐산물과 코-고곤제(D-serine 또는 glycine)의 동시 결합을 필요로 합니다.
- ^ 검토 결과, 마그네슘 L-아스파르트산과 염화마그네슘은 중독성 [108]행동에 중요한 변화를 일으키며, 다른 형태의 마그네슘은 언급되지 않았습니다.
- ^ 95% 신뢰 구간은 실제 사망자 수가 3,425명에서 4,145명 사이에 있을 확률이 95%임을 나타냅니다.
- ^ 인간 도파민 수송체는 아연 결합 시 도파민 재흡수를 억제하고 암페타민 유도 도파민 방출을 시험관 [147][148][149]내에서 증폭시키는 고친화성 세포 외 아연 결합 부위를 포함합니다.인간 세로토닌 수송체와 노르에피네프린 수송체는 아연 결합 [149]부위를 포함하지 않습니다.
- ^ 4-하이드록시암페타민은 시험관 내에서 도파민 베타-하이드록시실라아제(DBH)에 의해 4-하이드록시노레페드린으로 대사되는 것으로 나타났으며,[167][170] 생체 내에서도 유사하게 대사되는 것으로 추정됩니다.혈청 DBH 농도가 인간의 4-하이드록시암페타민 대사에 미치는 영향을 측정한 연구의 증거는 다른 효소가 4-하이드록시암페타민의 [170][172]4-하이드록시노레페드린으로의 전환을 매개할 수 있음을 시사합니다.동물 연구로부터의 다른 증거는 이 반응이 [173][174]뇌의 노르아드레날린 뉴런 안의 시냅스 소포에서 DBH에 의해 촉매된다는 것을 암시합니다.
- ^ 해부학적 [175][176]부위별로 마이크로바이옴 조성과 미생물 농도에 상당한 차이가 있습니다.어떤 해부학적 부위에서도 가장 많은 미생물을 함유하고 있는 인간 대장에서 나온 액체는 약 1조 개(10^12개)의 박테리아 세포/[175]ml를 포함하고 있습니다.
- ^ 균일성을 위해 Lenntech 분자량 계산기를[188] 사용하여 몰 질량을 계산했으며 발표된 약학적 값의 0.01 g/mol 이내였습니다.
- ^ 암페타민 기준 백분율 = 분자량/분자량.애더럴의 암페타민 기준 백분율 = 성분 백분율의 합 / 4.
- ^ 선량 = (1 / 암페타민 기준 백분율) × 스케일링 인자 = (분자량 / 분자량) × 스케일링 인자.이 칼럼의 값은 30 mg 용량의 덱스트로암페타민 황산염으로 축척되었습니다.이러한 의약품 간의 약리학적 차이(예: 방출, 흡수, 전환, 농도의 차이, 에난티오머의 다양한 효과, 반감기 등)로 인해 나열된 값은 등용성 용량으로 간주되어서는 안 됩니다.
- 이미지 범례
참고문헌
- ^ [12][13][14][15][16][17][18][19][20][21][22]
- ^ [23][24][25][26][27][28][29][30]
- ^ [7][16][27][86][87][88]
- ^ [89][90][91][92]
- ^ [16][93][89][91]
- ^ [12][16][27][94]
- ^ a b [111][112][113][114][134]
- ^ [109][111][110][118][119]
- ^ [110][121][122][123]
- ^ [142][79][140][139][143]
- ^ a b [159][167][168][145][169][162][170][171]
참고문헌
- ^ a b c d Heal DJ, Smith SL, Gosden J, Nutt DJ (June 2013). "Amphetamine, past and present--a pharmacological and clinical perspective". Journal of Psychopharmacology. 27 (6): 479–496. doi:10.1177/0269881113482532. PMC 3666194. PMID 23539642.
- ^ a b Joyce BM, Glaser PE, Gerhardt GA (April 2007). "Adderall produces increased striatal dopamine release and a prolonged time course compared to amphetamine isomers". Psychopharmacology. 191 (3): 669–677. doi:10.1007/s00213-006-0550-9. PMID 17031708. S2CID 20283057.
- ^ Vitiello B (April 2008). "Understanding the risk of using medications for attention deficit hyperactivity disorder with respect to physical growth and cardiovascular function". Child and Adolescent Psychiatric Clinics of North America. 17 (2): 459–74, xi. doi:10.1016/j.chc.2007.11.010. PMC 2408826. PMID 18295156.
- ^ Graham J, Banaschewski T, Buitelaar J, Coghill D, Danckaerts M, Dittmann RW, et al. (January 2011). "European guidelines on managing adverse effects of medication for ADHD". European Child & Adolescent Psychiatry. 20 (1): 17–37. doi:10.1007/s00787-010-0140-6. eISSN 1435-165X. PMC 3012210. PMID 21042924.
- ^ Kociancic T, Reed MD, Findling RL (March 2004). "Evaluation of risks associated with short- and long-term psychostimulant therapy for treatment of ADHD in children". Expert Opinion on Drug Safety. 3 (2): 93–100. doi:10.1517/14740338.3.2.93. eISSN 1744-764X. PMID 15006715. S2CID 31114829.
- ^ Clemow DB, Walker DJ (September 2014). "The potential for misuse and abuse of medications in ADHD: a review". Postgraduate Medicine. 126 (5): 64–81. doi:10.3810/pgm.2014.09.2801. eISSN 1941-9260. PMID 25295651. S2CID 207580823.
- ^ a b c d e Stahl SM (March 2017). "Amphetamine (D,L)". Prescriber's Guide: Stahl's Essential Psychopharmacology (6th ed.). Cambridge, United Kingdom: Cambridge University Press. pp. 45–51. ISBN 9781108228749. Retrieved 5 August 2017.
- ^ a b Sagonowsky E (28 August 2017). "Shire launches new ADHD drug Mydayis as it weighs a neuroscience exit". Fierce Pharma. Questex LLC. Archived from the original on 16 December 2019. Retrieved 2 May 2020.
- ^ a b c d e f "National Drug Code Amphetamine Search Results". National Drug Code Directory. United States Food and Drug Administration. Archived from the original on 16 December 2013. Retrieved 16 December 2013.
- ^ "Pharmacology". Evekeo CII (amphetamine sulfate) HCP. Arbor Pharmaceuticals, LLC. Archived from the original on 21 September 2020. Retrieved 2 May 2020.
- ^ "Prescribing Information & Medication Guide" (PDF). Zenzedi (dextroamphetamine sulfate, USP). Arbor Pharmaceuticals LLC. Archived (PDF) from the original on 11 November 2020. Retrieved 2 May 2020.
- ^ a b Montgomery KA (June 2008). "Sexual desire disorders". Psychiatry. 5 (6): 50–55. PMC 2695750. PMID 19727285.
- ^ a b c d "Adderall- dextroamphetamine saccharate, amphetamine aspartate, dextroamphetamine sulfate, and amphetamine sulfate tablet". DailyMed. Teva Pharmaceuticals USA, Inc. 8 November 2019. Archived from the original on 2 October 2019. Retrieved 22 December 2019.
- ^ a b c d e f g Malenka RC, Nestler EJ, Hyman SE (2009). "Chapter 13: Higher Cognitive Function and Behavioral Control". In Sydor A, Brown RY (eds.). Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd ed.). New York, USA: McGraw-Hill Medical. pp. 318, 321. ISBN 9780071481274.
Therapeutic (relatively low) doses of psychostimulants, such as methylphenidate and amphetamine, improve performance on working memory tasks both in normal subjects and those with ADHD. ... stimulants act not only on working memory function, but also on general levels of arousal and, within the nucleus accumbens, improve the saliency of tasks. Thus, stimulants improve performance on effortful but tedious tasks ... through indirect stimulation of dopamine and norepinephrine receptors. ...
Beyond these general permissive effects, dopamine (acting via D1 receptors) and norepinephrine (acting at several receptors) can, at optimal levels, enhance working memory and aspects of attention. - ^ a b c d Liddle DG, Connor DJ (June 2013). "Nutritional supplements and ergogenic AIDS". Primary Care: Clinics in Office Practice. 40 (2): 487–505. doi:10.1016/j.pop.2013.02.009. PMID 23668655.
Amphetamines and caffeine are stimulants that increase alertness, improve focus, decrease reaction time, and delay fatigue, allowing for an increased intensity and duration of training ...
Physiologic and performance effects
• Amphetamines increase dopamine/norepinephrine release and inhibit their reuptake, leading to central nervous system (CNS) stimulation
• Amphetamines seem to enhance athletic performance in anaerobic conditions 39 40
• Improved reaction time
• Increased muscle strength and delayed muscle fatigue
• Increased acceleration
• Increased alertness and attention to task - ^ a b c d e f g h i j k l m n o p "Adderall XR- dextroamphetamine sulfate, dextroamphetamine saccharate, amphetamine sulfate and amphetamine aspartate capsule, extended release". DailyMed. Shire US Inc. 17 July 2019. Retrieved 22 December 2019.
- ^ a b Shoptaw SJ, Kao U, Ling W (January 2009). Shoptaw SJ, Ali R (ed.). "Treatment for amphetamine psychosis". Cochrane Database of Systematic Reviews. 2009 (1): CD003026. doi:10.1002/14651858.CD003026.pub3. PMC 7004251. PMID 19160215.
A minority of individuals who use amphetamines develop full-blown psychosis requiring care at emergency departments or psychiatric hospitals. In such cases, symptoms of amphetamine psychosis commonly include paranoid and persecutory delusions as well as auditory and visual hallucinations in the presence of extreme agitation. More common (about 18%) is for frequent amphetamine users to report psychotic symptoms that are sub-clinical and that do not require high-intensity intervention ...
About 5–15% of the users who develop an amphetamine psychosis fail to recover completely (Hofmann 1983) ...
Findings from one trial indicate use of antipsychotic medications effectively resolves symptoms of acute amphetamine psychosis.
psychotic symptoms of individuals with amphetamine psychosis may be due exclusively to heavy use of the drug or heavy use of the drug may exacerbate an underlying vulnerability to schizophrenia. - ^ a b Greydanus D. "Stimulant Misuse: Strategies to Manage a Growing Problem" (PDF). American College Health Association (Review Article). ACHA Professional Development Program. p. 20. Archived from the original (PDF) on 3 November 2013. Retrieved 2 November 2013.
- ^ a b Malenka RC, Nestler EJ, Hyman SE, Holtzman DM (2015). "Chapter 16: Reinforcement and Addictive Disorders". Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (3rd ed.). New York: McGraw-Hill Medical. ISBN 9780071827706.
Such agents also have important therapeutic uses; cocaine, for example, is used as a local anesthetic (Chapter 2), and amphetamines and methylphenidate are used in low doses to treat attention deficit hyperactivity disorder and in higher doses to treat narcolepsy (Chapter 12). Despite their clinical uses, these drugs are strongly reinforcing, and their long-term use at high doses is linked with potential addiction, especially when they are rapidly administered or when high-potency forms are given.
- ^ a b Kollins SH (May 2008). "A qualitative review of issues arising in the use of psycho-stimulant medications in patients with ADHD and co-morbid substance use disorders". Current Medical Research and Opinion. 24 (5): 1345–1357. doi:10.1185/030079908X280707. PMID 18384709. S2CID 71267668.
When oral formulations of psychostimulants are used at recommended doses and frequencies, they are unlikely to yield effects consistent with abuse potential in patients with ADHD.
- ^ Stolerman IP (2010). Stolerman IP (ed.). Encyclopedia of Psychopharmacology. Berlin, Germany; London, England: Springer. p. 78. ISBN 9783540686989.
- ^ Howell LL, Kimmel HL (January 2008). "Monoamine transporters and psychostimulant addiction". Biochemical Pharmacology. 75 (1): 196–217. doi:10.1016/j.bcp.2007.08.003. PMID 17825265.
- ^ a b c d e Malenka RC, Nestler EJ, Hyman SE (2009). "Chapter 6: Widely Projecting Systems: Monoamines, Acetylcholine, and Orexin". In Sydor A, Brown RY (eds.). Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd ed.). New York, USA: McGraw-Hill Medical. pp. 154–157. ISBN 9780071481274.
- ^ a b c d e f g h i j k l m Miller GM (January 2011). "The emerging role of trace amine-associated receptor 1 in the functional regulation of monoamine transporters and dopaminergic activity". J. Neurochem. 116 (2): 164–76. doi:10.1111/j.1471-4159.2010.07109.x. PMC 3005101. PMID 21073468.
- ^ a b c d e f g Eiden LE, Weihe E (January 2011). "VMAT2: a dynamic regulator of brain monoaminergic neuronal function interacting with drugs of abuse". Ann. N. Y. Acad. Sci. 1216 (1): 86–98. Bibcode:2011NYASA1216...86E. doi:10.1111/j.1749-6632.2010.05906.x. PMC 4183197. PMID 21272013.
VMAT2 is the CNS vesicular transporter for not only the biogenic amines DA, NE, EPI, 5-HT, and HIS, but likely also for the trace amines TYR, PEA, and thyronamine (THYR) ... [Trace aminergic] neurons in mammalian CNS would be identifiable as neurons expressing VMAT2 for storage, and the biosynthetic enzyme aromatic amino acid decarboxylase (AADC).
- ^ a b c d e f Broadley KJ (March 2010). "The vascular effects of trace amines and amphetamines". Pharmacology & Therapeutics. 125 (3): 363–375. doi:10.1016/j.pharmthera.2009.11.005. PMID 19948186.
- ^ a b c d e f g h i j k l m n o p q r s t u v Westfall DP, Westfall TC (2010). "Miscellaneous Sympathomimetic Agonists". In Brunton LL, Chabner BA, Knollmann BC (eds.). Goodman & Gilman's Pharmacological Basis of Therapeutics (12th ed.). New York, USA: McGraw-Hill. ISBN 9780071624428.
- ^ a b c d e Lewin AH, Miller GM, Gilmour B (December 2011). "Trace amine-associated receptor 1 is a stereoselective binding site for compounds in the amphetamine class". Bioorg. Med. Chem. 19 (23): 7044–7048. doi:10.1016/j.bmc.2011.10.007. PMC 3236098. PMID 22037049.
- ^ a b Anthony E (11 November 2013). Explorations in Child Psychiatry. Springer Science & Business Media. pp. 93–94. ISBN 9781468421279. Archived from the original on 21 May 2016. Retrieved 28 April 2015.
- ^ a b Arnold LE (2000). "Methyiphenidate vs. Amphetamine: Comparative review". Journal of Attention Disorders. 3 (4): 200–211. doi:10.1177/108705470000300403. S2CID 15901046.
- ^ "The Top 300 Drugs of 2020". ClinCalc. Retrieved 7 October 2022.
- ^ "Dextroamphetamine; Dextroamphetamine Saccharate; Amphetamine; Amphetamine Aspartate - Drug Usage Statistics". ClinCalc. Retrieved 7 October 2022.
- ^ Heal DJ, Smith SL, Gosden J, Nutt DJ (June 2013). "Amphetamine, past and present – a pharmacological and clinical perspective". Journal of Psychopharmacology. 27 (6): 479–496. doi:10.1177/0269881113482532. PMC 3666194. PMID 23539642.
The intravenous use of d-amphetamine and other stimulants still pose major safety risks to the individuals indulging in this practice. Some of this intravenous abuse is derived from the diversion of ampoules of d-amphetamine, which are still occasionally prescribed in the UK for the control of severe narcolepsy and other disorders of excessive sedation. ... For these reasons, observations of dependence and abuse of prescription d-amphetamine are rare in clinical practice, and this stimulant can even be prescribed to people with a history of drug abuse provided certain controls, such as daily pick-ups of prescriptions, are put in place (Jasinski and Krishnan, 2009b).
- ^ Carvalho M, Carmo H, Costa VM, Capela JP, Pontes H, Remião F, Carvalho F, Bastos Mde L (August 2012). "Toxicity of amphetamines: an update". Archives of Toxicology. 86 (8): 1167–1231. doi:10.1007/s00204-012-0815-5. PMID 22392347. S2CID 2873101.
- ^ Berman S, O'Neill J, Fears S, Bartzokis G, London ED (October 2008). "Abuse of amphetamines and structural abnormalities in the brain". Annals of the New York Academy of Sciences. 1141 (1): 195–220. doi:10.1196/annals.1441.031. PMC 2769923. PMID 18991959.
- ^ a b Hart H, Radua J, Nakao T, Mataix-Cols D, Rubia K (February 2013). "Meta-analysis of functional magnetic resonance imaging studies of inhibition and attention in attention-deficit/hyperactivity disorder: exploring task-specific, stimulant medication, and age effects". JAMA Psychiatry. 70 (2): 185–198. doi:10.1001/jamapsychiatry.2013.277. PMID 23247506.
- ^ a b Spencer TJ, Brown A, Seidman LJ, Valera EM, Makris N, Lomedico A, Faraone SV, Biederman J (September 2013). "Effect of psychostimulants on brain structure and function in ADHD: a qualitative literature review of magnetic resonance imaging-based neuroimaging studies". The Journal of Clinical Psychiatry. 74 (9): 902–917. doi:10.4088/JCP.12r08287. PMC 3801446. PMID 24107764.
- ^ a b Frodl T, Skokauskas N (February 2012). "Meta-analysis of structural MRI studies in children and adults with attention deficit hyperactivity disorder indicates treatment effects". Acta Psychiatrica Scandinavica. 125 (2): 114–126. doi:10.1111/j.1600-0447.2011.01786.x. PMID 22118249. S2CID 25954331.
Basal ganglia regions like the right globus pallidus, the right putamen, and the nucleus caudatus are structurally affected in children with ADHD. These changes and alterations in limbic regions like ACC and amygdala are more pronounced in non-treated populations and seem to diminish over time from child to adulthood. Treatment seems to have positive effects on brain structure.
- ^ a b c d e f Huang YS, Tsai MH (July 2011). "Long-term outcomes with medications for attention-deficit hyperactivity disorder: current status of knowledge". CNS Drugs. 25 (7): 539–554. doi:10.2165/11589380-000000000-00000. PMID 21699268. S2CID 3449435.
Several other studies,[97-101] including a meta-analytic review[98] and a retrospective study,[97] suggested that stimulant therapy in childhood is associated with a reduced risk of subsequent substance use, cigarette smoking and alcohol use disorders. ... Recent studies have demonstrated that stimulants, along with the non-stimulants atomoxetine and extended-release guanfacine, are continuously effective for more than 2-year treatment periods with few and tolerable adverse effects. The effectiveness of long-term therapy includes not only the core symptoms of ADHD, but also improved quality of life and academic achievements. The most concerning short-term adverse effects of stimulants, such as elevated blood pressure and heart rate, waned in long-term follow-up studies. ... The current data do not support the potential impact of stimulants on the worsening or development of tics or substance abuse into adulthood. In the longest follow-up study (of more than 10 years), lifetime stimulant treatment for ADHD was effective and protective against the development of adverse psychiatric disorders.
- ^ a b c Millichap JG (2010). "Chapter 9: Medications for ADHD". In Millichap JG (ed.). Attention Deficit Hyperactivity Disorder Handbook: A Physician's Guide to ADHD (2nd ed.). New York, USA: Springer. pp. 121–123, 125–127. ISBN 9781441913968.
Ongoing research has provided answers to many of the parents' concerns, and has confirmed the effectiveness and safety of the long-term use of medication.
- ^ a b c d e Arnold LE, Hodgkins P, Caci H, Kahle J, Young S (February 2015). "Effect of treatment modality on long-term outcomes in attention-deficit/hyperactivity disorder: a systematic review". PLOS ONE. 10 (2): e0116407. doi:10.1371/journal.pone.0116407. PMC 4340791. PMID 25714373.
The highest proportion of improved outcomes was reported with combination treatment (83% of outcomes). Among significantly improved outcomes, the largest effect sizes were found for combination treatment. The greatest improvements were associated with academic, self-esteem, or social function outcomes.
그림 3: 치료 종류별, 결과군별 치료 혜택 - ^ a b Bidwell LC, McClernon FJ, Kollins SH (August 2011). "Cognitive enhancers for the treatment of ADHD". Pharmacology Biochemistry and Behavior. 99 (2): 262–274. doi:10.1016/j.pbb.2011.05.002. PMC 3353150. PMID 21596055.
- ^ Parker J, Wales G, Chalhoub N, Harpin V (September 2013). "The long-term outcomes of interventions for the management of attention-deficit hyperactivity disorder in children and adolescents: a systematic review of randomized controlled trials". Psychology Research and Behavior Management. 6: 87–99. doi:10.2147/PRBM.S49114. PMC 3785407. PMID 24082796.
Only one paper53 examining outcomes beyond 36 months met the review criteria. ... There is high level evidence suggesting that pharmacological treatment can have a major beneficial effect on the core symptoms of ADHD (hyperactivity, inattention, and impulsivity) in approximately 80% of cases compared with placebo controls, in the short term.
- ^ Millichap JG (2010). "Chapter 9: Medications for ADHD". In Millichap JG (ed.). Attention Deficit Hyperactivity Disorder Handbook: A Physician's Guide to ADHD (2nd ed.). New York, USA: Springer. pp. 111–113. ISBN 9781441913968.
- ^ "Stimulants for Attention Deficit Hyperactivity Disorder". WebMD. Healthwise. 12 April 2010. Retrieved 12 November 2013.
- ^ Scholten RJ, Clarke M, Hetherington J (August 2005). "The Cochrane Collaboration". European Journal of Clinical Nutrition. 59 (Suppl 1): S147–S149, discussion S195–S196. doi:10.1038/sj.ejcn.1602188. PMID 16052183. S2CID 29410060.
- ^ a b Castells X, Blanco-Silvente L, Cunill R (August 2018). "Amphetamines for attention deficit hyperactivity disorder (ADHD) in adults". Cochrane Database of Systematic Reviews. 2018 (8): CD007813. doi:10.1002/14651858.CD007813.pub3. PMC 6513464. PMID 30091808.
- ^ Punja S, Shamseer L, Hartling L, Urichuk L, Vandermeer B, Nikles J, Vohra S (February 2016). "Amphetamines for attention deficit hyperactivity disorder (ADHD) in children and adolescents". Cochrane Database of Systematic Reviews. 2016 (2): CD009996. doi:10.1002/14651858.CD009996.pub2. PMC 10329868. PMID 26844979.
- ^ Osland ST, Steeves TD, Pringsheim T (June 2018). "Pharmacological treatment for attention deficit hyperactivity disorder (ADHD) in children with comorbid tic disorders". Cochrane Database of Systematic Reviews. 2018 (6): CD007990. doi:10.1002/14651858.CD007990.pub3. PMC 6513283. PMID 29944175.
- ^ a b c d "Adderall XR Prescribing Information" (PDF). United States Food and Drug Administration. Shire US Inc. December 2013. Archived (PDF) from the original on 30 December 2013. Retrieved 30 December 2013.
- ^ Truven Health Analytics. "Amphetamine/Dextroamphetamine (By mouth)". PubMed Health. Micromedex Consumer Medication Information. Archived from the original on 11 October 2014. Retrieved 4 September 2015.
- ^ "Generic Adderall Availability". Drugs.com. Archived from the original on 28 May 2020. Retrieved 6 February 2020.
- ^ "Generic Adderall XR Availability". Drugs.com. Archived from the original on 6 February 2020. Retrieved 6 February 2020.
- ^ a b Spencer RC, Devilbiss DM, Berridge CW (June 2015). "The Cognition-Enhancing Effects of Psychostimulants Involve Direct Action in the Prefrontal Cortex". Biological Psychiatry. 77 (11): 940–950. doi:10.1016/j.biopsych.2014.09.013. PMC 4377121. PMID 25499957.
The procognitive actions of psychostimulants are only associated with low doses. Surprisingly, despite nearly 80 years of clinical use, the neurobiology of the procognitive actions of psychostimulants has only recently been systematically investigated. Findings from this research unambiguously demonstrate that the cognition-enhancing effects of psychostimulants involve the preferential elevation of catecholamines in the PFC and the subsequent activation of norepinephrine α2 and dopamine D1 receptors. ... This differential modulation of PFC-dependent processes across dose appears to be associated with the differential involvement of noradrenergic α2 versus α1 receptors. Collectively, this evidence indicates that at low, clinically relevant doses, psychostimulants are devoid of the behavioral and neurochemical actions that define this class of drugs and instead act largely as cognitive enhancers (improving PFC-dependent function). ... In particular, in both animals and humans, lower doses maximally improve performance in tests of working memory and response inhibition, whereas maximal suppression of overt behavior and facilitation of attentional processes occurs at higher doses.
- ^ Ilieva IP, Hook CJ, Farah MJ (June 2015). "Prescription Stimulants' Effects on Healthy Inhibitory Control, Working Memory, and Episodic Memory: A Meta-analysis". Journal of Cognitive Neuroscience. 27 (6): 1069–1089. doi:10.1162/jocn_a_00776. PMID 25591060. S2CID 15788121.
Specifically, in a set of experiments limited to high-quality designs, we found significant enhancement of several cognitive abilities. ... The results of this meta-analysis ... do confirm the reality of cognitive enhancing effects for normal healthy adults in general, while also indicating that these effects are modest in size.
- ^ Bagot KS, Kaminer Y (April 2014). "Efficacy of stimulants for cognitive enhancement in non-attention deficit hyperactivity disorder youth: a systematic review". Addiction. 109 (4): 547–557. doi:10.1111/add.12460. PMC 4471173. PMID 24749160.
Amphetamine has been shown to improve consolidation of information (0.02 ≥ P ≤ 0.05), leading to improved recall.
- ^ Devous MD, Trivedi MH, Rush AJ (April 2001). "Regional cerebral blood flow response to oral amphetamine challenge in healthy volunteers". Journal of Nuclear Medicine. 42 (4): 535–542. PMID 11337538.
- ^ Malenka RC, Nestler EJ, Hyman SE (2009). "Chapter 10: Neural and Neuroendocrine Control of the Internal Milieu". In Sydor A, Brown RY (eds.). Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd ed.). New York, USA: McGraw-Hill Medical. p. 266. ISBN 9780071481274.
Dopamine acts in the nucleus accumbens to attach motivational significance to stimuli associated with reward.
- ^ a b c Wood S, Sage JR, Shuman T, Anagnostaras SG (January 2014). "Psychostimulants and cognition: a continuum of behavioral and cognitive activation". Pharmacological Reviews. 66 (1): 193–221. doi:10.1124/pr.112.007054. PMC 3880463. PMID 24344115.
- ^ Twohey M (26 March 2006). "Pills become an addictive study aid". JS Online. Archived from the original on 15 August 2007. Retrieved 2 December 2007.
- ^ Teter CJ, McCabe SE, LaGrange K, Cranford JA, Boyd CJ (October 2006). "Illicit use of specific prescription stimulants among college students: prevalence, motives, and routes of administration". Pharmacotherapy. 26 (10): 1501–1510. doi:10.1592/phco.26.10.1501. PMC 1794223. PMID 16999660.
- ^ Weyandt LL, Oster DR, Marraccini ME, Gudmundsdottir BG, Munro BA, Zavras BM, Kuhar B (September 2014). "Pharmacological interventions for adolescents and adults with ADHD: stimulant and nonstimulant medications and misuse of prescription stimulants". Psychology Research and Behavior Management. 7: 223–249. doi:10.2147/PRBM.S47013. PMC 4164338. PMID 25228824.
misuse of prescription stimulants has become a serious problem on college campuses across the US and has been recently documented in other countries as well. ... Indeed, large numbers of students claim to have engaged in the nonmedical use of prescription stimulants, which is reflected in lifetime prevalence rates of prescription stimulant misuse ranging from 5% to nearly 34% of students.
- ^ Clemow DB, Walker DJ (September 2014). "The potential for misuse and abuse of medications in ADHD: a review". Postgraduate Medicine. 126 (5): 64–81. doi:10.3810/pgm.2014.09.2801. PMID 25295651. S2CID 207580823.
Overall, the data suggest that ADHD medication misuse and diversion are common health care problems for stimulant medications, with the prevalence believed to be approximately 5% to 10% of high school students and 5% to 35% of college students, depending on the study.
- ^ Bracken NM (January 2012). "National Study of Substance Use Trends Among NCAA College Student-Athletes" (PDF). NCAA Publications. National Collegiate Athletic Association. Archived (PDF) from the original on 9 October 2022. Retrieved 8 October 2013.
- ^ Docherty JR (June 2008). "Pharmacology of stimulants prohibited by the World Anti-Doping Agency (WADA)". British Journal of Pharmacology. 154 (3): 606–622. doi:10.1038/bjp.2008.124. PMC 2439527. PMID 18500382.
- ^ a b c d Parr JW (July 2011). "Attention-deficit hyperactivity disorder and the athlete: new advances and understanding". Clinics in Sports Medicine. 30 (3): 591–610. doi:10.1016/j.csm.2011.03.007. PMID 21658550.
In 1980, Chandler and Blair47 showed significant increases in knee extension strength, acceleration, anaerobic capacity, time to exhaustion during exercise, pre-exercise and maximum heart rates, and time to exhaustion during maximal oxygen consumption (VO2 max) testing after administration of 15 mg of dextroamphetamine versus placebo. Most of the information to answer this question has been obtained in the past decade through studies of fatigue rather than an attempt to systematically investigate the effect of ADHD drugs on exercise.
- ^ a b c Roelands B, de Koning J, Foster C, Hettinga F, Meeusen R (May 2013). "Neurophysiological determinants of theoretical concepts and mechanisms involved in pacing". Sports Medicine. 43 (5): 301–311. doi:10.1007/s40279-013-0030-4. PMID 23456493. S2CID 30392999.
In high-ambient temperatures, dopaminergic manipulations clearly improve performance. The distribution of the power output reveals that after dopamine reuptake inhibition, subjects are able to maintain a higher power output compared with placebo. ... Dopaminergic drugs appear to override a safety switch and allow athletes to use a reserve capacity that is 'off-limits' in a normal (placebo) situation.
- ^ Parker KL, Lamichhane D, Caetano MS, Narayanan NS (October 2013). "Executive dysfunction in Parkinson's disease and timing deficits". Frontiers in Integrative Neuroscience. 7: 75. doi:10.3389/fnint.2013.00075. PMC 3813949. PMID 24198770.
Manipulations of dopaminergic signaling profoundly influence interval timing, leading to the hypothesis that dopamine influences internal pacemaker, or "clock," activity. For instance, amphetamine, which increases concentrations of dopamine at the synaptic cleft advances the start of responding during interval timing, whereas antagonists of D2 type dopamine receptors typically slow timing;... Depletion of dopamine in healthy volunteers impairs timing, while amphetamine releases synaptic dopamine and speeds up timing.
- ^ Rattray B, Argus C, Martin K, Northey J, Driller M (March 2015). "Is it time to turn our attention toward central mechanisms for post-exertional recovery strategies and performance?". Frontiers in Physiology. 6: 79. doi:10.3389/fphys.2015.00079. PMC 4362407. PMID 25852568.
Aside from accounting for the reduced performance of mentally fatigued participants, this model rationalizes the reduced RPE and hence improved cycling time trial performance of athletes using a glucose mouthwash (Chambers et al., 2009) and the greater power output during a RPE matched cycling time trial following amphetamine ingestion (Swart, 2009). ... Dopamine stimulating drugs are known to enhance aspects of exercise performance (Roelands et al., 2008)
- ^ Roelands B, De Pauw K, Meeusen R (June 2015). "Neurophysiological effects of exercise in the heat". Scandinavian Journal of Medicine & Science in Sports. 25 (Suppl 1): 65–78. doi:10.1111/sms.12350. PMID 25943657. S2CID 22782401.
This indicates that subjects did not feel they were producing more power and consequently more heat. The authors concluded that the "safety switch" or the mechanisms existing in the body to prevent harmful effects are overridden by the drug administration (Roelands et al., 2008b). Taken together, these data indicate strong ergogenic effects of an increased DA concentration in the brain, without any change in the perception of effort.
- ^ a b Moore DL. "Do pro sports leagues have an Adderall problem?". USA TODAY. Archived from the original on 23 November 2014. Retrieved 4 May 2014.
- ^ "Commonly Abused Prescription Drugs Chart". National Institute on Drug Abuse. Archived from the original on 1 May 2012. Retrieved 7 May 2012.
- ^ "Stimulant ADHD Medications – Methylphenidate and Amphetamines". National Institute on Drug Abuse. Archived from the original on 2 May 2012. Retrieved 7 May 2012.
- ^ a b c Abelman DD (6 October 2017). "Mitigating risks of students use of study drugs through understanding motivations for use and applying harm reduction theory: a literature review". Harm Reduction Journal. 14 (1): 68. doi:10.1186/s12954-017-0194-6. ISSN 1477-7517. PMC 5639593. PMID 28985738.
- ^ a b "National Institute on Drug Abuse. 2009. Stimulant ADHD Medications – Methylphenidate and Amphetamines". National Institute on Drug Abuse. Archived from the original on 12 March 2013. Retrieved 27 February 2013.
- ^ Kessler S (January 1996). "Drug therapy in attention-deficit hyperactivity disorder". Southern Medical Journal. 89 (1): 33–38. doi:10.1097/00007611-199601000-00005. PMID 8545689. S2CID 12798818.
statements on package inserts are not intended to limit medical practice. Rather they are intended to limit claims by pharmaceutical companies. ... the FDA asserts explicitly, and the courts have upheld that clinical decisions are to be made by physicians and patients in individual situations.
- ^ Heal DJ, Smith SL, Gosden J, Nutt DJ (June 2013). "Amphetamine, past and present – a pharmacological and clinical perspective". Journal of Psychopharmacology. 27 (6): 479–496. doi:10.1177/0269881113482532. PMC 3666194. PMID 23539642.
The intravenous use of d-amphetamine and other stimulants still pose major safety risks to the individuals indulging in this practice. Some of this intravenous abuse is derived from the diversion of ampoules of d-amphetamine, which are still occasionally prescribed in the UK for the control of severe narcolepsy and other disorders of excessive sedation. ... For these reasons, observations of dependence and abuse of prescription d-amphetamine are rare in clinical practice, and this stimulant can even be prescribed to people with a history of drug abuse provided certain controls, such as daily pick-ups of prescriptions, are put in place (Jasinski and Krishnan, 2009b).
- ^ a b c "Evekeo- amphetamine sulfate tablet". DailyMed. Arbor Pharmaceuticals, LLC. 14 August 2019. Retrieved 22 December 2019.
- ^ a b c d e f g h i "Adderall XR- dextroamphetamine sulfate, dextroamphetamine saccharate, amphetamine sulfate and amphetamine aspartate capsule, extended release". DailyMed. Shire US Inc. 17 July 2019. Retrieved 22 December 2019.
- ^ a b c d e f g h i j Heedes G, Ailakis J. "Amphetamine (PIM 934)". INCHEM. International Programme on Chemical Safety. Retrieved 24 June 2014.
- ^ Feinberg SS (November 2004). "Combining stimulants with monoamine oxidase inhibitors: a review of uses and one possible additional indication". The Journal of Clinical Psychiatry. 65 (11): 1520–1524. doi:10.4088/jcp.v65n1113. PMID 15554766.
- ^ Stewart JW, Deliyannides DA, McGrath PJ (June 2014). "How treatable is refractory depression?". Journal of Affective Disorders. 167: 148–152. doi:10.1016/j.jad.2014.05.047. PMID 24972362.
- ^ Huang YS, Tsai MH (July 2011). "Long-term outcomes with medications for attention-deficit hyperactivity disorder: current status of knowledge". CNS Drugs. 25 (7): 539–554. doi:10.2165/11589380-000000000-00000. PMID 21699268. S2CID 3449435.
Several other studies,[97-101] including a meta-analytic review[98] and a retrospective study,[97] suggested that stimulant therapy in childhood is associated with a reduced risk of subsequent substance use, cigarette smoking and alcohol use disorders. ... Recent studies have demonstrated that stimulants, along with the non-stimulants atomoxetine and extended-release guanfacine, are continuously effective for more than 2-year treatment periods with few and tolerable adverse effects. The effectiveness of long-term therapy includes not only the core symptoms of ADHD, but also improved quality of life and academic achievements. The most concerning short-term adverse effects of stimulants, such as elevated blood pressure and heart rate, waned in long-term follow-up studies. ... The current data do not support the potential impact of stimulants on the worsening or development of tics or substance abuse into adulthood. In the longest follow-up study (of more than 10 years), lifetime stimulant treatment for ADHD was effective and protective against the development of adverse psychiatric disorders.
- ^ Millichap JG (2010). "Chapter 9: Medications for ADHD". In Millichap JG (ed.). Attention Deficit Hyperactivity Disorder Handbook: A Physician's Guide to ADHD (2nd ed.). New York: Springer. p. 112. ISBN 9781441913968.
Table 9.2 Dextroamphetamine formulations of stimulant medication
Dexedrine [Peak:2–3 h] [Duration:5–6 h] ...
Adderall [Peak:2–3 h] [Duration:5–7 h]
Dexedrine spansules [Peak:7–8 h] [Duration:12 h] ...
Adderall XR [Peak:7–8 h] [Duration:12 h]
Vyvanse [Peak:3–4 h] [Duration:12 h] - ^ a b Vitiello B (April 2008). "Understanding the risk of using medications for attention deficit hyperactivity disorder with respect to physical growth and cardiovascular function". Child and Adolescent Psychiatric Clinics of North America. 17 (2): 459–474. doi:10.1016/j.chc.2007.11.010. PMC 2408826. PMID 18295156.
- ^ a b Vitiello B (April 2008). "Understanding the risk of using medications for attention deficit hyperactivity disorder with respect to physical growth and cardiovascular function". Child and Adolescent Psychiatric Clinics of North America. 17 (2): 459–474. doi:10.1016/j.chc.2007.11.010. PMC 2408826. PMID 18295156.
- ^ Ramey JT, Bailen E, Lockey RF (2006). "Rhinitis medicamentosa" (PDF). Journal of Investigational Allergology & Clinical Immunology. 16 (3): 148–155. PMID 16784007. Retrieved 29 April 2015.
Table 2. Decongestants Causing Rhinitis Medicamentosa
– Nasal decongestants:
– Sympathomimetic:
• Amphetamine - ^ a b "FDA Drug Safety Communication: Safety Review Update of Medications used to treat Attention-Deficit/Hyperactivity Disorder (ADHD) in children and young adults". United States Food and Drug Administration. 1 November 2011. Archived from the original on 25 August 2019. Retrieved 24 December 2019.
- ^ Cooper WO, Habel LA, Sox CM, Chan KA, Arbogast PG, Cheetham TC, Murray KT, Quinn VP, Stein CM, Callahan ST, Fireman BH, Fish FA, Kirshner HS, O'Duffy A, Connell FA, Ray WA (November 2011). "ADHD drugs and serious cardiovascular events in children and young adults". New England Journal of Medicine. 365 (20): 1896–1904. doi:10.1056/NEJMoa1110212. PMC 4943074. PMID 22043968.
- ^ a b "FDA Drug Safety Communication: Safety Review Update of Medications used to treat Attention-Deficit/Hyperactivity Disorder (ADHD) in adults". United States Food and Drug Administration. 12 December 2011. Archived from the original on 14 December 2019. Retrieved 24 December 2013.
- ^ Habel LA, Cooper WO, Sox CM, Chan KA, Fireman BH, Arbogast PG, Cheetham TC, Quinn VP, Dublin S, Boudreau DM, Andrade SE, Pawloski PA, Raebel MA, Smith DH, Achacoso N, Uratsu C, Go AS, Sidney S, Nguyen-Huynh MN, Ray WA, Selby JV (December 2011). "ADHD medications and risk of serious cardiovascular events in young and middle-aged adults". JAMA. 306 (24): 2673–2683. doi:10.1001/jama.2011.1830. PMC 3350308. PMID 22161946.
- ^ Heedes G, Ailakis J. "Amphetamine (PIM 934)". INCHEM. International Programme on Chemical Safety. Retrieved 24 June 2014.
- ^ O'Connor PG (February 2012). "Amphetamines". Merck Manual for Health Care Professionals. Merck. Retrieved 8 May 2012.
- ^ a b Bramness JG, Gundersen ØH, Guterstam J, Rognli EB, Konstenius M, Løberg EM, Medhus S, Tanum L, Franck J (December 2012). "Amphetamine-induced psychosis—a separate diagnostic entity or primary psychosis triggered in the vulnerable?". BMC Psychiatry. 12: 221. doi:10.1186/1471-244X-12-221. PMC 3554477. PMID 23216941.
In these studies, amphetamine was given in consecutively higher doses until psychosis was precipitated, often after 100–300 mg of amphetamine ... Secondly, psychosis has been viewed as an adverse event, although rare, in children with ADHD who have been treated with amphetamine
- ^ a b Childs E, de Wit H (May 2009). "Amphetamine-induced place preference in humans". Biological Psychiatry. 65 (10): 900–904. doi:10.1016/j.biopsych.2008.11.016. PMC 2693956. PMID 19111278.
This study demonstrates that humans, like nonhumans, prefer a place associated with amphetamine administration. These findings support the idea that subjective responses to a drug contribute to its ability to establish place conditioning.
- ^ a b Malenka RC, Nestler EJ, Hyman SE (2009). "Chapter 15: Reinforcement and Addictive Disorders". In Sydor A, Brown RY (eds.). Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd ed.). New York: McGraw-Hill Medical. pp. 364–375. ISBN 9780071481274.
- ^ a b c d e Nestler EJ (December 2013). "Cellular basis of memory for addiction". Dialogues in Clinical Neuroscience. 15 (4): 431–443. PMC 3898681. PMID 24459410.
Despite the importance of numerous psychosocial factors, at its core, drug addiction involves a biological process: the ability of repeated exposure to a drug of abuse to induce changes in a vulnerable brain that drive the compulsive seeking and taking of drugs, and loss of control over drug use, that define a state of addiction. ... A large body of literature has demonstrated that such ΔFosB induction in D1-type [nucleus accumbens] neurons increases an animal's sensitivity to drug as well as natural rewards and promotes drug self-administration, presumably through a process of positive reinforcement ... Another ΔFosB target is cFos: as ΔFosB accumulates with repeated drug exposure it represses c-Fos and contributes to the molecular switch whereby ΔFosB is selectively induced in the chronic drug-treated state.41. ... Moreover, there is increasing evidence that, despite a range of genetic risks for addiction across the population, exposure to sufficiently high doses of a drug for long periods of time can transform someone who has relatively lower genetic loading into an addict.
- ^ Volkow ND, Koob GF, McLellan AT (January 2016). "Neurobiologic Advances from the Brain Disease Model of Addiction". New England Journal of Medicine. 374 (4): 363–371. doi:10.1056/NEJMra1511480. PMC 6135257. PMID 26816013.
Substance-use disorder: A diagnostic term in the fifth edition of the Diagnostic and Statistical Manual of Mental Disorders (DSM-5) referring to recurrent use of alcohol or other drugs that causes clinically and functionally significant impairment, such as health problems, disability, and failure to meet major responsibilities at work, school, or home. Depending on the level of severity, this disorder is classified as mild, moderate, or severe.
Addiction: A term used to indicate the most severe, chronic stage of substance-use disorder, in which there is a substantial loss of self-control, as indicated by compulsive drug taking despite the desire to stop taking the drug. In the DSM-5, the term addiction is synonymous with the classification of severe substance-use disorder. - ^ a b c Renthal W, Nestler EJ (September 2009). "Chromatin regulation in drug addiction and depression". Dialogues in Clinical Neuroscience. 11 (3): 257–268. PMC 2834246. PMID 19877494.
[Psychostimulants] increase cAMP levels in striatum, which activates protein kinase A (PKA) and leads to phosphorylation of its targets. This includes the cAMP response element binding protein (CREB), the phosphorylation of which induces its association with the histone acetyltransferase, CREB binding protein (CBP) to acetylate histones and facilitate gene activation. This is known to occur on many genes including fosB and c-fos in response to psychostimulant exposure. ΔFosB is also upregulated by chronic psychostimulant treatments, and is known to activate certain genes (eg, cdk5) and repress others (eg, c-fos) where it recruits HDAC1 as a corepressor. ... Chronic exposure to psychostimulants increases glutamatergic [signaling] from the prefrontal cortex to the NAc. Glutamatergic signaling elevates Ca2+ levels in NAc postsynaptic elements where it activates CaMK (calcium/calmodulin protein kinases) signaling, which, in addition to phosphorylating CREB, also phosphorylates HDAC5.
그림 2: 정신 자극제에 의한 신호 전달 사건 - ^ Broussard JI (January 2012). "Co-transmission of dopamine and glutamate". The Journal of General Physiology. 139 (1): 93–96. doi:10.1085/jgp.201110659. PMC 3250102. PMID 22200950.
Coincident and convergent input often induces plasticity on a postsynaptic neuron. The NAc integrates processed information about the environment from basolateral amygdala, hippocampus, and prefrontal cortex (PFC), as well as projections from midbrain dopamine neurons. Previous studies have demonstrated how dopamine modulates this integrative process. For example, high frequency stimulation potentiates hippocampal inputs to the NAc while simultaneously depressing PFC synapses (Goto and Grace, 2005). The converse was also shown to be true; stimulation at PFC potentiates PFC–NAc synapses but depresses hippocampal–NAc synapses. In light of the new functional evidence of midbrain dopamine/glutamate co-transmission (references above), new experiments of NAc function will have to test whether midbrain glutamatergic inputs bias or filter either limbic or cortical inputs to guide goal-directed behavior.
- ^ Kanehisa Laboratories (10 October 2014). "Amphetamine – Homo sapiens (human)". KEGG Pathway. Retrieved 31 October 2014.
Most addictive drugs increase extracellular concentrations of dopamine (DA) in nucleus accumbens (NAc) and medial prefrontal cortex (mPFC), projection areas of mesocorticolimbic DA neurons and key components of the "brain reward circuit". Amphetamine achieves this elevation in extracellular levels of DA by promoting efflux from synaptic terminals. ... Chronic exposure to amphetamine induces a unique transcription factor delta FosB, which plays an essential role in long-term adaptive changes in the brain.
- ^ Cadet JL, Brannock C, Jayanthi S, Krasnova IN (2015). "Transcriptional and epigenetic substrates of methamphetamine addiction and withdrawal: evidence from a long-access self-administration model in the rat". Molecular Neurobiology. 51 (2): 696–717 (Figure 1). doi:10.1007/s12035-014-8776-8. PMC 4359351. PMID 24939695.
- ^ a b c Robison AJ, Nestler EJ (November 2011). "Transcriptional and epigenetic mechanisms of addiction". Nature Reviews Neuroscience. 12 (11): 623–637. doi:10.1038/nrn3111. PMC 3272277. PMID 21989194.
ΔFosB serves as one of the master control proteins governing this structural plasticity. ... ΔFosB also represses G9a expression, leading to reduced repressive histone methylation at the cdk5 gene. The net result is gene activation and increased CDK5 expression. ... In contrast, ΔFosB binds to the c-fos gene and recruits several co-repressors, including HDAC1 (histone deacetylase 1) and SIRT 1 (sirtuin 1). ... The net result is c-fos gene repression.
그림 4: 유전자 발현 약물 조절의 후생유전학적 기초 - ^ a b c Nestler EJ (December 2012). "Transcriptional mechanisms of drug addiction". Clinical Psychopharmacology and Neuroscience. 10 (3): 136–143. doi:10.9758/cpn.2012.10.3.136. PMC 3569166. PMID 23430970.
The 35-37 kD ΔFosB isoforms accumulate with chronic drug exposure due to their extraordinarily long half-lives. ... As a result of its stability, the ΔFosB protein persists in neurons for at least several weeks after cessation of drug exposure. ... ΔFosB overexpression in nucleus accumbens induces NFκB ... In contrast, the ability of ΔFosB to repress the c-Fos gene occurs in concert with the recruitment of a histone deacetylase and presumably several other repressive proteins such as a repressive histone methyltransferase
- ^ Nestler EJ (October 2008). "Transcriptional mechanisms of addiction: Role of ΔFosB". Philosophical Transactions of the Royal Society B: Biological Sciences. 363 (1507): 3245–3255. doi:10.1098/rstb.2008.0067. PMC 2607320. PMID 18640924.
Recent evidence has shown that ΔFosB also represses the c-fos gene that helps create the molecular switch—from the induction of several short-lived Fos family proteins after acute drug exposure to the predominant accumulation of ΔFosB after chronic drug exposure
- ^ Kanehisa Laboratories (10 October 2014). "Amphetamine – Homo sapiens (human)". KEGG Pathway. Retrieved 31 October 2014.
- ^ a b c d e f Nechifor M (March 2008). "Magnesium in drug dependences". Magnesium Research. 21 (1): 5–15. doi:10.1684/mrh.2008.0124 (inactive 1 August 2023). PMID 18557129.
{{cite journal}}: CS1 메인 : 2023년 8월 기준 DOI 비활성화 (링크) - ^ a b c d e Ruffle JK (November 2014). "Molecular neurobiology of addiction: what's all the (Δ)FosB about?". The American Journal of Drug and Alcohol Abuse. 40 (6): 428–437. doi:10.3109/00952990.2014.933840. PMID 25083822. S2CID 19157711.
ΔFosB is an essential transcription factor implicated in the molecular and behavioral pathways of addiction following repeated drug exposure.
- ^ a b c d e f g h i j k Robison AJ, Nestler EJ (November 2011). "Transcriptional and epigenetic mechanisms of addiction". Nature Reviews Neuroscience. 12 (11): 623–637. doi:10.1038/nrn3111. PMC 3272277. PMID 21989194.
ΔFosB has been linked directly to several addiction-related behaviors ... Importantly, genetic or viral overexpression of ΔJunD, a dominant negative mutant of JunD which antagonizes ΔFosB- and other AP-1-mediated transcriptional activity, in the NAc or OFC blocks these key effects of drug exposure14,22–24. This indicates that ΔFosB is both necessary and sufficient for many of the changes wrought in the brain by chronic drug exposure. ΔFosB is also induced in D1-type NAc MSNs by chronic consumption of several natural rewards, including sucrose, high fat food, sex, wheel running, where it promotes that consumption14,26–30. This implicates ΔFosB in the regulation of natural rewards under normal conditions and perhaps during pathological addictive-like states. ... ΔFosB serves as one of the master control proteins governing this structural plasticity.
- ^ a b c d e f g h i j k l m n o p q r s t u v Olsen CM (December 2011). "Natural rewards, neuroplasticity, and non-drug addictions". Neuropharmacology. 61 (7): 1109–1122. doi:10.1016/j.neuropharm.2011.03.010. PMC 3139704. PMID 21459101.
Similar to environmental enrichment, studies have found that exercise reduces self-administration and relapse to drugs of abuse (Cosgrove et al., 2002; Zlebnik et al., 2010). There is also some evidence that these preclinical findings translate to human populations, as exercise reduces withdrawal symptoms and relapse in abstinent smokers (Daniel et al., 2006; Prochaska et al., 2008), and one drug recovery program has seen success in participants that train for and compete in a marathon as part of the program (Butler, 2005). ... In humans, the role of dopamine signaling in incentive-sensitization processes has recently been highlighted by the observation of a dopamine dysregulation syndrome in some patients taking dopaminergic drugs. This syndrome is characterized by a medication-induced increase in (or compulsive) engagement in non-drug rewards such as gambling, shopping, or sex (Evans et al., 2006; Aiken, 2007; Lader, 2008).
- ^ a b c d Lynch WJ, Peterson AB, Sanchez V, Abel J, Smith MA (September 2013). "Exercise as a novel treatment for drug addiction: a neurobiological and stage-dependent hypothesis". Neuroscience & Biobehavioral Reviews. 37 (8): 1622–1644. doi:10.1016/j.neubiorev.2013.06.011. PMC 3788047. PMID 23806439.
These findings suggest that exercise may "magnitude"-dependently prevent the development of an addicted phenotype possibly by blocking/reversing behavioral and neuroadaptive changes that develop during and following extended access to the drug. ... Exercise has been proposed as a treatment for drug addiction that may reduce drug craving and risk of relapse. Although few clinical studies have investigated the efficacy of exercise for preventing relapse, the few studies that have been conducted generally report a reduction in drug craving and better treatment outcomes ... Taken together, these data suggest that the potential benefits of exercise during relapse, particularly for relapse to psychostimulants, may be mediated via chromatin remodeling and possibly lead to greater treatment outcomes.
- ^ a b c Zhou Y, Zhao M, Zhou C, Li R (July 2015). "Sex differences in drug addiction and response to exercise intervention: From human to animal studies". Frontiers in Neuroendocrinology. 40: 24–41. doi:10.1016/j.yfrne.2015.07.001. PMC 4712120. PMID 26182835.
Collectively, these findings demonstrate that exercise may serve as a substitute or competition for drug abuse by changing ΔFosB or cFos immunoreactivity in the reward system to protect against later or previous drug use. ... The postulate that exercise serves as an ideal intervention for drug addiction has been widely recognized and used in human and animal rehabilitation.
- ^ a b c Linke SE, Ussher M (January 2015). "Exercise-based treatments for substance use disorders: evidence, theory, and practicality". The American Journal of Drug and Alcohol Abuse. 41 (1): 7–15. doi:10.3109/00952990.2014.976708. PMC 4831948. PMID 25397661.
The limited research conducted suggests that exercise may be an effective adjunctive treatment for SUDs. In contrast to the scarce intervention trials to date, a relative abundance of literature on the theoretical and practical reasons supporting the investigation of this topic has been published. ... numerous theoretical and practical reasons support exercise-based treatments for SUDs, including psychological, behavioral, neurobiological, nearly universal safety profile, and overall positive health effects.
- ^ Hyman SE, Malenka RC, Nestler EJ (July 2006). "Neural mechanisms of addiction: the role of reward-related learning and memory" (PDF). Annual Review of Neuroscience. 29: 565–598. doi:10.1146/annurev.neuro.29.051605.113009. PMID 16776597. S2CID 15139406. Archived from the original (PDF) on 19 September 2018.
- ^ a b c d e Steiner H, Van Waes V (January 2013). "Addiction-related gene regulation: risks of exposure to cognitive enhancers vs. other psychostimulants". Progress in Neurobiology. 100: 60–80. doi:10.1016/j.pneurobio.2012.10.001. PMC 3525776. PMID 23085425.
- ^ Malenka RC, Nestler EJ, Hyman SE (2009). "Chapter 4: Signal Transduction in the Brain". In Sydor A, Brown RY (eds.). Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd ed.). New York, USA: McGraw-Hill Medical. p. 94. ISBN 9780071481274.
- ^ Kanehisa Laboratories (29 October 2014). "Alcoholism – Homo sapiens (human)". KEGG Pathway. Retrieved 31 October 2014.
- ^ Kim Y, Teylan MA, Baron M, Sands A, Nairn AC, Greengard P (February 2009). "Methylphenidate-induced dendritic spine formation and DeltaFosB expression in nucleus accumbens". Proceedings of the National Academy of Sciences. 106 (8): 2915–2920. Bibcode:2009PNAS..106.2915K. doi:10.1073/pnas.0813179106. PMC 2650365. PMID 19202072.
- ^ a b Nestler EJ (January 2014). "Epigenetic mechanisms of drug addiction". Neuropharmacology. 76 (Pt B): 259–268. doi:10.1016/j.neuropharm.2013.04.004. PMC 3766384. PMID 23643695.
- ^ a b Biliński P, Wojtyła A, Kapka-Skrzypczak L, Chwedorowicz R, Cyranka M, Studziński T (2012). "Epigenetic regulation in drug addiction". Annals of Agricultural and Environmental Medicine. 19 (3): 491–496. PMID 23020045.
- ^ Kennedy PJ, Feng J, Robison AJ, Maze I, Badimon A, Mouzon E, Chaudhury D, Damez-Werno DM, Haggarty SJ, Han MH, Bassel-Duby R, Olson EN, Nestler EJ (April 2013). "Class I HDAC inhibition blocks cocaine-induced plasticity by targeted changes in histone methylation". Nature Neuroscience. 16 (4): 434–440. doi:10.1038/nn.3354. PMC 3609040. PMID 23475113.
- ^ Whalley K (December 2014). "Psychiatric disorders: a feat of epigenetic engineering". Nature Reviews. Neuroscience. 15 (12): 768–769. doi:10.1038/nrn3869. PMID 25409693. S2CID 11513288.
- ^ a b Blum K, Werner T, Carnes S, Carnes P, Bowirrat A, Giordano J, Oscar-Berman M, Gold M (March 2012). "Sex, drugs, and rock 'n' roll: hypothesizing common mesolimbic activation as a function of reward gene polymorphisms". Journal of Psychoactive Drugs. 44 (1): 38–55. doi:10.1080/02791072.2012.662112. PMC 4040958. PMID 22641964.
It has been found that deltaFosB gene in the NAc is critical for reinforcing effects of sexual reward. Pitchers and colleagues (2010) reported that sexual experience was shown to cause DeltaFosB accumulation in several limbic brain regions including the NAc, medial pre-frontal cortex, VTA, caudate, and putamen, but not the medial preoptic nucleus. ... these findings support a critical role for DeltaFosB expression in the NAc in the reinforcing effects of sexual behavior and sexual experience-induced facilitation of sexual performance. ... both drug addiction and sexual addiction represent pathological forms of neuroplasticity along with the emergence of aberrant behaviors involving a cascade of neurochemical changes mainly in the brain's rewarding circuitry.
- ^ Pitchers KK, Vialou V, Nestler EJ, Laviolette SR, Lehman MN, Coolen LM (February 2013). "Natural and drug rewards act on common neural plasticity mechanisms with ΔFosB as a key mediator". The Journal of Neuroscience. 33 (8): 3434–3442. doi:10.1523/JNEUROSCI.4881-12.2013. PMC 3865508. PMID 23426671.
- ^ Beloate LN, Weems PW, Casey GR, Webb IC, Coolen LM (February 2016). "Nucleus accumbens NMDA receptor activation regulates amphetamine cross-sensitization and deltaFosB expression following sexual experience in male rats". Neuropharmacology. 101: 154–164. doi:10.1016/j.neuropharm.2015.09.023. PMID 26391065. S2CID 25317397.
- ^ Malenka RC, Nestler EJ, Hyman SE, Holtzman DM (2015). "Chapter 16: Reinforcement and Addictive Disorders". Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (3rd ed.). New York: McGraw-Hill Medical. ISBN 9780071827706.
Pharmacologic treatment for psychostimulant addiction is generally unsatisfactory. As previously discussed, cessation of cocaine use and the use of other psychostimulants in dependent individuals does not produce a physical withdrawal syndrome but may produce dysphoria, anhedonia, and an intense desire to reinitiate drug use.
- ^ a b c d Chan B, Freeman M, Kondo K, Ayers C, Montgomery J, Paynter R, Kansagara D (December 2019). "Pharmacotherapy for methamphetamine/amphetamine use disorder-a systematic review and meta-analysis". Addiction. 114 (12): 2122–2136. doi:10.1111/add.14755. PMID 31328345. S2CID 198136436.
- ^ Stoops WW, Rush CR (May 2014). "Combination pharmacotherapies for stimulant use disorder: a review of clinical findings and recommendations for future research". Expert Review of Clinical Pharmacology. 7 (3): 363–374. doi:10.1586/17512433.2014.909283. PMC 4017926. PMID 24716825.
Despite concerted efforts to identify a pharmacotherapy for managing stimulant use disorders, no widely effective medications have been approved.
- ^ a b Grandy DK, Miller GM, Li JX (February 2016). ""TAARgeting Addiction"-The Alamo Bears Witness to Another Revolution: An Overview of the Plenary Symposium of the 2015 Behavior, Biology and Chemistry Conference". Drug and Alcohol Dependence. 159: 9–16. doi:10.1016/j.drugalcdep.2015.11.014. PMC 4724540. PMID 26644139.
When considered together with the rapidly growing literature in the field a compelling case emerges in support of developing TAAR1-selective agonists as medications for preventing relapse to psychostimulant abuse.
- ^ a b Jing L, Li JX (August 2015). "Trace amine-associated receptor 1: A promising target for the treatment of psychostimulant addiction". European Journal of Pharmacology. 761: 345–352. doi:10.1016/j.ejphar.2015.06.019. PMC 4532615. PMID 26092759.
Existing data provided robust preclinical evidence supporting the development of TAAR1 agonists as potential treatment for psychostimulant abuse and addiction.
- ^ a b Malenka RC, Nestler EJ, Hyman SE (2009). "Chapter 5: Excitatory and Inhibitory Amino Acids". In Sydor A, Brown RY (eds.). Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd ed.). New York, USA: McGraw-Hill Medical. pp. 124–125. ISBN 9780071481274.
- ^ a b c Carroll ME, Smethells JR (February 2016). "Sex Differences in Behavioral Dyscontrol: Role in Drug Addiction and Novel Treatments". Frontiers in Psychiatry. 6: 175. doi:10.3389/fpsyt.2015.00175. PMC 4745113. PMID 26903885.
Physical Exercise
There is accelerating evidence that physical exercise is a useful treatment for preventing and reducing drug addiction ... In some individuals, exercise has its own rewarding effects, and a behavioral economic interaction may occur, such that physical and social rewards of exercise can substitute for the rewarding effects of drug abuse. ... The value of this form of treatment for drug addiction in laboratory animals and humans is that exercise, if it can substitute for the rewarding effects of drugs, could be self-maintained over an extended period of time. Work to date in [laboratory animals and humans] regarding exercise as a treatment for drug addiction supports this hypothesis. ... Animal and human research on physical exercise as a treatment for stimulant addiction indicates that this is one of the most promising treatments on the horizon. - ^ Perez-Mana C, Castells X, Torrens M, Capella D, Farre M (September 2013). "Efficacy of psychostimulant drugs for amphetamine abuse or dependence". Cochrane Database of Systematic Reviews. 9 (9): CD009695. doi:10.1002/14651858.CD009695.pub2. PMID 23996457.
- ^ "Amphetamines: Drug Use and Abuse". Merck Manual Home Edition. Merck. February 2003. Archived from the original on 17 February 2007. Retrieved 28 February 2007.
- ^ a b c d Shoptaw SJ, Kao U, Heinzerling K, Ling W (April 2009). Shoptaw SJ (ed.). "Treatment for amphetamine withdrawal". Cochrane Database of Systematic Reviews. 2009 (2): CD003021. doi:10.1002/14651858.CD003021.pub2. PMC 7138250. PMID 19370579.
The prevalence of this withdrawal syndrome is extremely common (Cantwell 1998; Gossop 1982) with 87.6% of 647 individuals with amphetamine dependence reporting six or more signs of amphetamine withdrawal listed in the DSM when the drug is not available (Schuckit 1999) ... The severity of withdrawal symptoms is greater in amphetamine dependent individuals who are older and who have more extensive amphetamine use disorders (McGregor 2005). Withdrawal symptoms typically present within 24 hours of the last use of amphetamine, with a withdrawal syndrome involving two general phases that can last 3 weeks or more. The first phase of this syndrome is the initial "crash" that resolves within about a week (Gossop 1982;McGregor 2005) ...
- ^ Stahl SM (March 2017). "Amphetamine (D,L)". Prescriber's Guide: Stahl's Essential Psychopharmacology (6th ed.). Cambridge, United Kingdom: Cambridge University Press. pp. 45–51. ISBN 9781108228749. Retrieved 5 August 2017.
- ^ a b Spiller HA, Hays HL, Aleguas A (June 2013). "Overdose of drugs for attention-deficit hyperactivity disorder: clinical presentation, mechanisms of toxicity, and management". CNS Drugs. 27 (7): 531–543. doi:10.1007/s40263-013-0084-8. PMID 23757186. S2CID 40931380.
Amphetamine, dextroamphetamine, and methylphenidate act as substrates for the cellular monoamine transporter, especially the dopamine transporter (DAT) and less so the norepinephrine (NET) and serotonin transporter. The mechanism of toxicity is primarily related to excessive extracellular dopamine, norepinephrine, and serotonin.
- ^ a b c d Westfall DP, Westfall TC (2010). "Miscellaneous Sympathomimetic Agonists". In Brunton LL, Chabner BA, Knollmann BC (eds.). Goodman & Gilman's Pharmacological Basis of Therapeutics (12th ed.). New York, USA: McGraw-Hill. ISBN 9780071624428.
- ^ Collaborators (2015). "Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990–2013: a systematic analysis for the Global Burden of Disease Study 2013". The Lancet. 385 (9963): 117–171. doi:10.1016/S0140-6736(14)61682-2. hdl:11655/15525. PMC 4340604. PMID 25530442.
Amphetamine use disorders ... 3,788 (3,425–4,145)
- ^ Greene SL, Kerr F, Braitberg G (October 2008). "Review article: amphetamines and related drugs of abuse". Emergency Medicine Australasia. 20 (5): 391–402. doi:10.1111/j.1742-6723.2008.01114.x. PMID 18973636. S2CID 20755466.
- ^ Albertson TE (2011). "Amphetamines". In Olson KR, Anderson IB, Benowitz NL, Blanc PD, Kearney TE, Kim-Katz SY, Wu AH (eds.). Poisoning & Drug Overdose (6th ed.). New York: McGraw-Hill Medical. pp. 77–79. ISBN 9780071668330.
- ^ a b c d e "Adderall XR Prescribing Information" (PDF). United States Food and Drug Administration. December 2013. pp. 8–10. Archived (PDF) from the original on 30 December 2013. Retrieved 30 December 2013.
- ^ a b Krueger SK, Williams DE (June 2005). "Mammalian flavin-containing monooxygenases: structure/function, genetic polymorphisms and role in drug metabolism". Pharmacology & Therapeutics. 106 (3): 357–387. doi:10.1016/j.pharmthera.2005.01.001. PMC 1828602. PMID 15922018.
표 5: N-함유 약물 및 FMO에 의해 산소화된 이종 생물학적 물질 - ^ a b c "Mydayis Prescribing Information" (PDF). United States Food and Drug Administration. Shire US Inc. June 2017. pp. 1–21. Archived (PDF) from the original on 9 June 2019. Retrieved 8 August 2017.
- ^ Krause J (April 2008). "SPECT and PET of the dopamine transporter in attention-deficit/hyperactivity disorder". Expert Rev. Neurother. 8 (4): 611–625. doi:10.1586/14737175.8.4.611. PMID 18416663. S2CID 24589993.
Zinc binds at ... extracellular sites of the DAT [103], serving as a DAT inhibitor. In this context, controlled double-blind studies in children are of interest, which showed positive effects of zinc [supplementation] on symptoms of ADHD [105,106]. It should be stated that at this time [supplementation] with zinc is not integrated in any ADHD treatment algorithm.
- ^ Sulzer D (February 2011). "How addictive drugs disrupt presynaptic dopamine neurotransmission". Neuron. 69 (4): 628–649. doi:10.1016/j.neuron.2011.02.010. PMC 3065181. PMID 21338876.
They did not confirm the predicted straightforward relationship between uptake and release, but rather that some compounds including AMPH were better releasers than substrates for uptake. Zinc, moreover, stimulates efflux of intracellular [3H]DA despite its concomitant inhibition of uptake (Scholze et al., 2002).
- ^ a b Scholze P, Nørregaard L, Singer EA, Freissmuth M, Gether U, Sitte HH (June 2002). "The role of zinc ions in reverse transport mediated by monoamine transporters". J. Biol. Chem. 277 (24): 21505–21513. doi:10.1074/jbc.M112265200. PMID 11940571.
The human dopamine transporter (hDAT) contains an endogenous high affinity Zn2+ binding site with three coordinating residues on its extracellular face (His193, His375, and Glu396). ... Although Zn2+ inhibited uptake, Zn2+ facilitated [3H]MPP+ release induced by amphetamine, MPP+, or K+-induced depolarization specifically at hDAT but not at the human serotonin and the norepinephrine transporter (hNET). ... Surprisingly, this amphetamine-elicited efflux was markedly enhanced, rather than inhibited, by the addition of 10 μM Zn2+ to the superfusion buffer (Fig. 2 A, open squares). We stress that Zn2+ per se did not affect basal efflux (Fig. 2 A). ... In many brain regions, Zn2+ is stored in synaptic vesicles and co-released together with glutamate; under basal conditions, the extracellular levels of Zn2+ are low (~10 nM; see Refs. 39, 40). Upon neuronal stimulation, however, Zn2+ is co-released with the neurotransmitters and, consequently, the free Zn2+ concentration may transiently reach values that range from 10–20 μM (10) up to 300 μM (11). The concentrations of Zn2+ shown in this study, required for the stimulation of dopamine release (as well as inhibition of uptake), covered this physiologically relevant range, with maximum stimulation occurring at 3–30 μM. It is therefore conceivable that the action of Zn2+ on hDAT does not merely reflect a biochemical peculiarity but that it is physiologically relevant. ... Thus, when Zn2+ is co-released with glutamate, it may greatly augment the efflux of dopamine.
- ^ Scassellati C, Bonvicini C, Faraone SV, Gennarelli M (October 2012). "Biomarkers and attention-deficit/hyperactivity disorder: a systematic review and meta-analyses". J. Am. Acad. Child Adolesc. Psychiatry. 51 (10): 1003–1019.e20. doi:10.1016/j.jaac.2012.08.015. PMID 23021477.
Although we did not find a sufficient number of studies suitable for a meta-analysis of PEA and ADHD, three studies20,57,58 confirmed that urinary levels of PEA were significantly lower in patients with ADHD compared with controls. ... Administration of D-amphetamine and methylphenidate resulted in a markedly increased urinary excretion of PEA,20,60 suggesting that ADHD treatments normalize PEA levels. ... Similarly, urinary biogenic trace amine PEA levels could be a biomarker for the diagnosis of ADHD,20,57,58 for treatment efficacy,20,60 and associated with symptoms of inattentivenesss.59 ... With regard to zinc supplementation, a placebo controlled trial reported that doses up to 30 mg/day of zinc were safe for at least 8 weeks, but the clinical effect was equivocal except for the finding of a 37% reduction in amphetamine optimal dose with 30 mg per day of zinc.110
- ^ Sulzer D, Cragg SJ, Rice ME (August 2016). "Striatal dopamine neurotransmission: regulation of release and uptake". Basal Ganglia. 6 (3): 123–148. doi:10.1016/j.baga.2016.02.001. PMC 4850498. PMID 27141430.
Despite the challenges in determining synaptic vesicle pH, the proton gradient across the vesicle membrane is of fundamental importance for its function. Exposure of isolated catecholamine vesicles to protonophores collapses the pH gradient and rapidly redistributes transmitter from inside to outside the vesicle. ... Amphetamine and its derivatives like methamphetamine are weak base compounds that are the only widely used class of drugs known to elicit transmitter release by a non-exocytic mechanism. As substrates for both DAT and VMAT, amphetamines can be taken up to the cytosol and then sequestered in vesicles, where they act to collapse the vesicular pH gradient.
- ^ Ledonne A, Berretta N, Davoli A, Rizzo GR, Bernardi G, Mercuri NB (July 2011). "Electrophysiological effects of trace amines on mesencephalic dopaminergic neurons". Front. Syst. Neurosci. 5: 56. doi:10.3389/fnsys.2011.00056. PMC 3131148. PMID 21772817.
Three important new aspects of TAs action have recently emerged: (a) inhibition of firing due to increased release of dopamine; (b) reduction of D2 and GABAB receptor-mediated inhibitory responses (excitatory effects due to disinhibition); and (c) a direct TA1 receptor-mediated activation of GIRK channels which produce cell membrane hyperpolarization.
- ^ "TAAR1". GenAtlas. University of Paris. 28 January 2012. Retrieved 29 May 2014.
• tonically activates inwardly rectifying K(+) channels, which reduces the basal firing frequency of dopamine (DA) neurons of the ventral tegmental area (VTA)
- ^ Underhill SM, Wheeler DS, Li M, Watts SD, Ingram SL, Amara SG (July 2014). "Amphetamine modulates excitatory neurotransmission through endocytosis of the glutamate transporter EAAT3 in dopamine neurons". Neuron. 83 (2): 404–416. doi:10.1016/j.neuron.2014.05.043. PMC 4159050. PMID 25033183.
AMPH also increases intracellular calcium (Gnegy et al., 2004) that is associated with calmodulin/CamKII activation (Wei et al., 2007) and modulation and trafficking of the DAT (Fog et al., 2006; Sakrikar et al., 2012). ... For example, AMPH increases extracellular glutamate in various brain regions including the striatum, VTA and NAc (Del Arco et al., 1999; Kim et al., 1981; Mora and Porras, 1993; Xue et al., 1996), but it has not been established whether this change can be explained by increased synaptic release or by reduced clearance of glutamate. ... DHK-sensitive, EAAT2 uptake was not altered by AMPH (Figure 1A). The remaining glutamate transport in these midbrain cultures is likely mediated by EAAT3 and this component was significantly decreased by AMPH
- ^ Vaughan RA, Foster JD (September 2013). "Mechanisms of dopamine transporter regulation in normal and disease states". Trends Pharmacol. Sci. 34 (9): 489–496. doi:10.1016/j.tips.2013.07.005. PMC 3831354. PMID 23968642.
AMPH and METH also stimulate DA efflux, which is thought to be a crucial element in their addictive properties [80], although the mechanisms do not appear to be identical for each drug [81]. These processes are PKCβ– and CaMK–dependent [72, 82], and PKCβ knock-out mice display decreased AMPH-induced efflux that correlates with reduced AMPH-induced locomotion [72].
- ^ "Amphetamine: Biomolecular Interactions and Pathways". PubChem Compound. National Center for Biotechnology Information. Archived from the original on 13 October 2013. Retrieved 13 October 2013.
- ^ Smith RC, Davis JM (June 1977). "Comparative effects of d-amphetamine, l-amphetamine, and methylphenidate on mood in man". Psychopharmacology. 53 (1): 1–12. doi:10.1007/bf00426687. PMID 407607. S2CID 37967136.
- ^ Wishart DS, Djombou Feunang Y, Guo AC, Lo EJ, Marcu A, Grant JR, Sajed T, Johnson D, Li C, Sayeeda Z, Assempour N, Iynkkaran I, Liu Y, Maciejewski A, Gale N, Wilson A, Chin L, Cummings R, Le D, Pon A, Knox C, Wilson M. "Dextroamphetamine DrugBank Online". DrugBank. 5.0.
- ^ a b c d e f g h i j k l m n "Adderall XR Prescribing Information" (PDF). United States Food and Drug Administration. Shire US Inc. December 2013. pp. 12–13. Retrieved 30 December 2013.
- ^ Wishart DS, Djombou Feunang Y, Guo AC, Lo EJ, Marcu A, Grant JR, Sajed T, Johnson D, Li C, Sayeeda Z, Assempour N, Iynkkaran I, Liu Y, Maciejewski A, Gale N, Wilson A, Chin L, Cummings R, Le D, Pon A, Knox C, Wilson M. "Amphetamine DrugBank Online". DrugBank. 5.0.
- ^ a b c d e "Metabolism/Pharmacokinetics". Amphetamine. Archived from the original on 2 October 2017. Retrieved 2 October 2017.
Duration of effect varies depending on agent and urine pH. Excretion is enhanced in more acidic urine. Half-life is 7 to 34 hours and is, in part, dependent on urine pH (half-life is longer with alkaline urine). ... Amphetamines are distributed into most body tissues with high concentrations occurring in the brain and CSF. Amphetamine appears in the urine within about 3 hours following oral administration. ... Three days after a dose of (+ or -)-amphetamine, human subjects had excreted 91% of the (14)C in the urine
{{cite encyclopedia}}:work=무시됨(도움말) - ^ a b c Santagati NA, Ferrara G, Marrazzo A, Ronsisvalle G (September 2002). "Simultaneous determination of amphetamine and one of its metabolites by HPLC with electrochemical detection". Journal of Pharmaceutical and Biomedical Analysis. 30 (2): 247–255. doi:10.1016/S0731-7085(02)00330-8. PMID 12191709.
- ^ "Compound Summary". p-Hydroxyamphetamine. Retrieved 15 October 2013.
{{cite encyclopedia}}:work=무시됨(도움말) - ^ "Compound Summary". p-Hydroxynorephedrine. Retrieved 15 October 2013.
{{cite encyclopedia}}:work=무시됨(도움말) - ^ "Compound Summary". Phenylpropanolamine. Retrieved 15 October 2013.
{{cite encyclopedia}}:work=무시됨(도움말) - ^ "Pharmacology and Biochemistry". Amphetamine. Retrieved 12 October 2013.
{{cite encyclopedia}}:work=무시됨(도움말) - ^ a b Glennon RA (2013). "Phenylisopropylamine stimulants: amphetamine-related agents". In Lemke TL, Williams DA, Roche VF, Zito W (eds.). Foye's principles of medicinal chemistry (7th ed.). Philadelphia, US: Wolters Kluwer Health/Lippincott Williams & Wilkins. pp. 646–648. ISBN 9781609133450.
The simplest unsubstituted phenylisopropylamine, 1-phenyl-2-aminopropane, or amphetamine, serves as a common structural template for hallucinogens and psychostimulants. Amphetamine produces central stimulant, anorectic, and sympathomimetic actions, and it is the prototype member of this class (39). ... The phase 1 metabolism of amphetamine analogs is catalyzed by two systems: cytochrome P450 and flavin monooxygenase. ... Amphetamine can also undergo aromatic hydroxylation to p-hydroxyamphetamine. ... Subsequent oxidation at the benzylic position by DA β-hydroxylase affords p-hydroxynorephedrine. Alternatively, direct oxidation of amphetamine by DA β-hydroxylase can afford norephedrine.
- ^ Taylor KB (January 1974). "Dopamine-beta-hydroxylase. Stereochemical course of the reaction" (PDF). Journal of Biological Chemistry. 249 (2): 454–458. PMID 4809526. Retrieved 6 November 2014.
Dopamine-β-hydroxylase catalyzed the removal of the pro-R hydrogen atom and the production of 1-norephedrine, (2S,1R)-2-amino-1-hydroxyl-1-phenylpropane, from d-amphetamine.
- ^ Cashman JR, Xiong YN, Xu L, Janowsky A (March 1999). "N-oxygenation of amphetamine and methamphetamine by the human flavin-containing monooxygenase (form 3): role in bioactivation and detoxication". Journal of Pharmacology and Experimental Therapeutics. 288 (3): 1251–1260. PMID 10027866.
- ^ a b c Sjoerdsma A, von Studnitz W (April 1963). "Dopamine-beta-oxidase activity in man, using hydroxyamphetamine as substrate". British Journal of Pharmacology and Chemotherapy. 20: 278–284. doi:10.1111/j.1476-5381.1963.tb01467.x. PMC 1703637. PMID 13977820.
Hydroxyamphetamine was administered orally to five human subjects ... Since conversion of hydroxyamphetamine to hydroxynorephedrine occurs in vitro by the action of dopamine-β-oxidase, a simple method is suggested for measuring the activity of this enzyme and the effect of its inhibitors in man. ... The lack of effect of administration of neomycin to one patient indicates that the hydroxylation occurs in body tissues. ... a major portion of the β-hydroxylation of hydroxyamphetamine occurs in non-adrenal tissue. Unfortunately, at the present time one cannot be completely certain that the hydroxylation of hydroxyamphetamine in vivo is accomplished by the same enzyme which converts dopamine to noradrenaline.
- ^ a b Badenhorst CP, van der Sluis R, Erasmus E, van Dijk AA (September 2013). "Glycine conjugation: importance in metabolism, the role of glycine N-acyltransferase, and factors that influence interindividual variation". Expert Opinion on Drug Metabolism & Toxicology. 9 (9): 1139–1153. doi:10.1517/17425255.2013.796929. PMID 23650932.
Figure 1. Glycine conjugation of benzoic acid. The glycine conjugation pathway consists of two steps. First benzoate is ligated to CoASH to form the high-energy benzoyl-CoA thioester. This reaction is catalyzed by the HXM-A and HXM-B medium-chain acid:CoA ligases and requires energy in the form of ATP. ... The benzoyl-CoA is then conjugated to glycine by GLYAT to form hippuric acid, releasing CoASH. In addition to the factors listed in the boxes, the levels of ATP, CoASH, and glycine may influence the overall rate of the glycine conjugation pathway.
- ^ Horwitz D, Alexander RW, Lovenberg W, Keiser HR (May 1973). "Human serum dopamine-β-hydroxylase. Relationship to hypertension and sympathetic activity". Circulation Research. 32 (5): 594–599. doi:10.1161/01.RES.32.5.594. PMID 4713201.
The biologic significance of the different levels of serum DβH activity was studied in two ways. First, in vivo ability to β-hydroxylate the synthetic substrate hydroxyamphetamine was compared in two subjects with low serum DβH activity and two subjects with average activity. ... In one study, hydroxyamphetamine (Paredrine), a synthetic substrate for DβH, was administered to subjects with either low or average levels of serum DβH activity. The percent of the drug hydroxylated to hydroxynorephedrine was comparable in all subjects (6.5-9.62) (Table 3).
- ^ Freeman JJ, Sulser F (December 1974). "Formation of p-hydroxynorephedrine in brain following intraventricular administration of p-hydroxyamphetamine". Neuropharmacology. 13 (12): 1187–1190. doi:10.1016/0028-3908(74)90069-0. PMID 4457764.
In species where aromatic hydroxylation of amphetamine is the major metabolic pathway, p-hydroxyamphetamine (POH) and p-hydroxynorephedrine (PHN) may contribute to the pharmacological profile of the parent drug. ... The location of the p-hydroxylation and β-hydroxylation reactions is important in species where aromatic hydroxylation of amphetamine is the predominant pathway of metabolism. Following systemic administration of amphetamine to rats, POH has been found in urine and in plasma.
The observed lack of a significant accumulation of PHN in brain following the intraventricular administration of (+)-amphetamine and the formation of appreciable amounts of PHN from (+)-POH in brain tissue in vivo supports the view that the aromatic hydroxylation of amphetamine following its systemic administration occurs predominantly in the periphery, and that POH is then transported through the blood-brain barrier, taken up by noradrenergic neurones in brain where (+)-POH is converted in the storage vesicles by dopamine β-hydroxylase to PHN. - ^ Matsuda LA, Hanson GR, Gibb JW (December 1989). "Neurochemical effects of amphetamine metabolites on central dopaminergic and serotonergic systems". Journal of Pharmacology and Experimental Therapeutics. 251 (3): 901–908. PMID 2600821.
The metabolism of p-OHA to p-OHNor is well documented and dopamine-β hydroxylase present in noradrenergic neurons could easily convert p-OHA to p-OHNor after intraventricular administration.
- ^ a b c d e f ElRakaiby M, Dutilh BE, Rizkallah MR, Boleij A, Cole JN, Aziz RK (July 2014). "Pharmacomicrobiomics: the impact of human microbiome variations on systems pharmacology and personalized therapeutics". Omics. 18 (7): 402–414. doi:10.1089/omi.2014.0018. PMC 4086029. PMID 24785449.
The hundred trillion microbes and viruses residing in every human body, which outnumber human cells and contribute at least 100 times more genes than those encoded on the human genome (Ley et al., 2006), offer an immense accessory pool for inter-individual genetic variation that has been underestimated and largely unexplored (Savage, 1977; Medini et al., 2008; Minot et al., 2011; Wylie et al., 2012). ... Meanwhile, a wealth of literature has long been available about the biotransformation of xenobiotics, notably by gut bacteria (reviewed in Sousa et al., 2008; Rizkallah et al., 2010; Johnson et al., 2012; Haiser and Turnbaugh, 2013). This valuable information is predominantly about drug metabolism by unknown human-associated microbes; however, only a few cases of inter-individual microbiome variations have been documented [e.g., digoxin (Mathan et al., 1989) and acetaminophen (Clayton et al., 2009)].
- ^ a b c Cho I, Blaser MJ (March 2012). "The human microbiome: at the interface of health and disease". Nature Reviews Genetics. 13 (4): 260–270. doi:10.1038/nrg3182. PMC 3418802. PMID 22411464.
The composition of the microbiome varies by anatomical site (Figure 1). The primary determinant of community composition is anatomical location: interpersonal variation is substantial23,24 and is higher than the temporal variability seen at most sites in a single individual25. ... How does the microbiome affect the pharmacology of medications? Can we "micro-type" people to improve pharmacokinetics and/or reduce toxicity? Can we manipulate the microbiome to improve pharmacokinetic stability?
- ^ Hutter T, Gimbert C, Bouchard F, Lapointe FJ (2015). "Being human is a gut feeling". Microbiome. 3: 9. doi:10.1186/s40168-015-0076-7. PMC 4359430. PMID 25774294.
Some metagenomic studies have suggested that less than 10% of the cells that comprise our bodies are Homo sapiens cells. The remaining 90% are bacterial cells. The description of this so-called human microbiome is of great interest and importance for several reasons. For one, it helps us redefine what a biological individual is. We suggest that a human individual is now best described as a super-individual in which a large number of different species (including Homo sapiens) coexist.
- ^ a b c d Kumar K, Dhoke GV, Sharma AK, Jaiswal SK, Sharma VK (January 2019). "Mechanistic elucidation of amphetamine metabolism by tyramine oxidase from human gut microbiota using molecular dynamics simulations". Journal of Cellular Biochemistry. 120 (7): 11206–11215. doi:10.1002/jcb.28396. PMID 30701587. S2CID 73413138.
Particularly in the case of the human gut, which harbors a large diversity of bacterial species, the differences in microbial composition can significantly alter the metabolic activity in the gut lumen.4 The differential metabolic activity due to the differences in gut microbial species has been recently linked with various metabolic disorders and diseases.5–12 In addition to the impact of gut microbial diversity or dysbiosis in various human diseases, there is an increasing amount of evidence which shows that the gut microbes can affect the bioavailability and efficacy of various orally administrated drug molecules through promiscuous enzymatic metabolism.13,14 ... The present study on the atomistic details of amphetamine binding and binding affinity to the tyramine oxidase along with the comparison with two natural substrates of this enzyme namely tyramine and phenylalanine provides strong evidence for the promiscuity-based metabolism of amphetamine by the tyramine oxidase enzyme of E. coli. The obtained results will be crucial in designing a surrogate molecule for amphetamine that can help either in improving the efficacy and bioavailability of the amphetamine drug via competitive inhibition or in redesigning the drug for better pharmacological effects. This study will also have useful clinical implications in reducing the gut microbiota caused variation in the drug response among different populations.
- ^ a b Khan MZ, Nawaz W (October 2016). "The emerging roles of human trace amines and human trace amine-associated receptors (hTAARs) in central nervous system". Biomedicine & Pharmacotherapy. 83: 439–449. doi:10.1016/j.biopha.2016.07.002. PMID 27424325.
- ^ a b c d e Lindemann L, Hoener MC (May 2005). "A renaissance in trace amines inspired by a novel GPCR family". Trends in Pharmacological Sciences. 26 (5): 274–281. doi:10.1016/j.tips.2005.03.007. PMID 15860375.
- ^ a b Schwarz A (14 December 2013). "The Selling of Attention Deficit Disorder". The New York Times. ISSN 0362-4331. Archived from the original on 1 March 2015. Retrieved 22 April 2017.
- ^ "(Collection of internal FDA information pertaining to the topic of Obetrol/Adderall)" (PDF). www.accessdata.fda.gov. US Food and Drug Administration. Archived (PDF) from the original on 17 May 2017. Retrieved 27 April 2017.
- ^ "REGULATORY NEWS: Richwood's Adderall". Health News Daily. 22 February 1996. Archived from the original on 23 May 2016. Retrieved 29 May 2013.
- ^ "APPROVAL LETTER" (PDF). United States Food and Drug Administration. Archived (PDF) from the original on 22 August 2013. Retrieved 30 December 2013.
- ^ "August 2006 News Archives: Barr and Shire Sign Three Agreements". GenericsWeb. Archived from the original on 8 February 2014. Retrieved 30 December 2013.
WOODCLIFF LAKE, N.J., Aug. 14 /PRNewswire-FirstCall/ – Barr Pharmaceuticals, Inc. today announced that its subsidiary Duramed Pharmaceuticals, Inc. and Shire plc have signed a Product Acquisition Agreement for ADDERALL(R) (immediate-release mixed amphetamine salts) tablets and a Product Development Agreement for six proprietary products, and that its subsidiary Barr Laboratories, Inc. (Barr) has signed a Settlement and License Agreement relating to the resolution of two pending patent cases involving Shire's ADDERALL XR(R) ...
- ^ "Teva Completes Acquisition of Barr". Drugs.com. Archived from the original on 8 March 2012. Retrieved 31 October 2011.
- ^ "Teva sells 1st generic of Adderall XL in US". Forbes Magazine. Associated Press. 2 April 2009. Archived from the original on 9 April 2009. Retrieved 22 April 2009.
- ^ "Molecular Weight Calculator". Lenntech. Retrieved 19 August 2015.
- ^ a b "Dextroamphetamine Sulfate USP". Mallinckrodt Pharmaceuticals. March 2014. Retrieved 19 August 2015.
- ^ a b "D-amphetamine sulfate". Tocris. 2015. Retrieved 19 August 2015.
- ^ a b "Amphetamine Sulfate USP". Mallinckrodt Pharmaceuticals. March 2014. Retrieved 19 August 2015.
- ^ "Dextroamphetamine Saccharate". Mallinckrodt Pharmaceuticals. March 2014. Retrieved 19 August 2015.
- ^ "Amphetamine Aspartate". Mallinckrodt Pharmaceuticals. March 2014. Retrieved 19 August 2015.
- ^ "Vyvanse Prescribing Information" (PDF). United States Food and Drug Administration. Shire US Inc. May 2017. pp. 17–21. Retrieved 10 July 2017.
- ^ "Controlled Drugs and Substances Act (S.C. 1996, c. 19)". 25 April 2017. Archived from the original on 3 April 2011. Retrieved 23 May 2013.
- ^ "Importing or Bringing Medication into Japan for Personal Use". Japan Ministry of Health, Labour and Welfare. Archived from the original on 13 July 2013. Retrieved 13 October 2013.
- ^ "Caught in the Dragnet". 2 August 2002. Archived from the original on 19 November 2018. Retrieved 18 November 2018.
- ^ "Thailand Law" (PDF). Government of Thailand. Archived from the original (PDF) on 8 March 2014. Retrieved 23 May 2013.
- ^ "Class A, B and C drugs". Home Office, Government of the United Kingdom. Archived from the original on 4 August 2007. Retrieved 23 July 2007.
- ^ Substance Abuse and Mental Health Services Administration. "Trends in Methamphetamine/Amphetamine Admissions to Treatment: 1993–2003". The Drug and Alcohol Services Information System (DASIS) Report. United States Department of Health and Human Services. Archived from the original on 5 March 2013. Retrieved 6 May 2016.
- ^ United Nations Office on Drugs and Crime (2007). Preventing Amphetamine-type Stimulant Use Among Young People: A Policy and Programming Guide (PDF). New York: United Nations. ISBN 978-92-1-148223-2. Archived (PDF) from the original on 16 October 2013. Retrieved 7 February 2012.
- ^ International Narcotics Control Board. "List of psychotropic substances under international control" (PDF). Vienna: United Nations. Archived from the original (PDF) on 5 December 2005. Retrieved 19 November 2005.
- ^ "The ADHD medication shortage is getting worse. What went wrong?—Neither drugmakers nor the DEA anticipated a sharp rise in ADHD diagnoses during the pandemic. Now an entire class of medications may be in short supply". NBC. 6 February 2023. Retrieved 25 February 2023.
- ^ "Adderall shortage raises questions about widespread dependency on the drug". PBS Newshour. 25 November 2022. Retrieved 25 February 2023.
- ^ Hart B (27 March 2023). "Where's the Urgency on the Adderall Shortage?". Intelligencer. Retrieved 27 March 2023.
- ^ "'Exciting Time': FDA Commissioner Talks AI and Misinformation". WebMD. 31 May 2023.
- ^ "FDA Commissioner Blames Adderall Shortage on Stimulant Overuse, Telehealth, Generics". Anni Layne Rodgers via Additidemag. 2 June 2023.
외부 링크
- "Amphetamine". Drug Information Portal. U.S. National Library of Medicine.
- "Amphetamine sulfate". Drug Information Portal. U.S. National Library of Medicine.
- "Amphetamine aspartate". Drug Information Portal. U.S. National Library of Medicine.
- "Dextroamphetamine saccharate". Drug Information Portal. U.S. National Library of Medicine.
- "Amphetamine". MedlinePlus.
- "Buy Adderall Online". Drug Information Portal. U.S. Pharmacy Store.